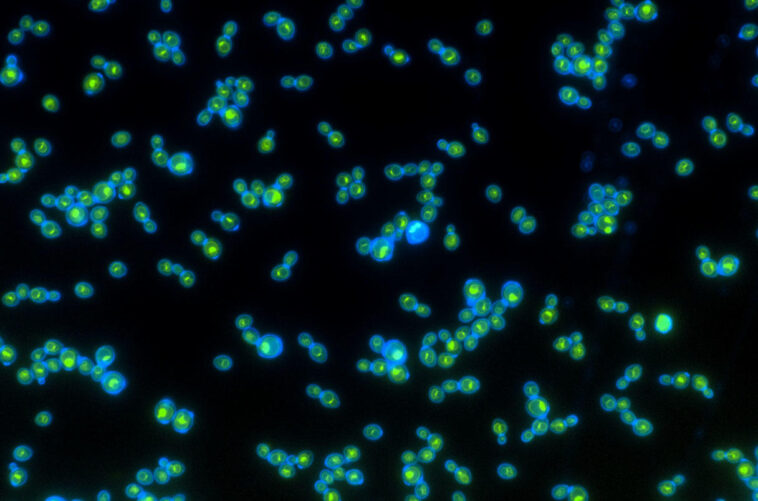
Les protéines de rhodopsine verte à l’intérieur des parois cellulaires bleues aident ces levures à se développer plus rapidement lorsqu’elles sont exposées à la lumière. Crédit : Anthony Burnetti, Georgia Institute of Technology
La levure est souvent connue pour sa capacité à fermenter les glucides en produits tels que le pain et la bière, nécessitant généralement un environnement sombre. L’exposition à la lumière dans ces situations peut perturber ou gâcher le processus de fermentation.
Cependant, une étude récente publiée dans Biologie actuelle par des chercheurs de l’École des sciences biologiques de Georgia Tech présente un développement révolutionnaire : ils ont mis au point l’une des premières souches de levure qui pourrait être plus heureuse lorsque les lumières sont allumées.
« Nous avons été franchement choqués par la simplicité avec laquelle il était possible de transformer la levure en phototrophes (des organismes capables d’exploiter et d’utiliser l’énergie de la lumière) », explique Anthony Burnetti, chercheur scientifique travaillant dans le laboratoire du professeur agrégé William Ratcliff et auteur correspondant de l’étude. « Tout ce que nous avions à faire était de déplacer un seul gène, et ils se sont développés 2 % plus rapidement à la lumière que dans l’obscurité. Sans aucun réglage ni aucune persuasion minutieuse, cela a simplement fonctionné.
Équiper facilement la levure d’un trait aussi important sur le plan évolutif pourrait signifier de grandes choses pour notre compréhension de l’origine de ce trait – et comment il peut être utilisé pour étudier des éléments tels que la production de biocarburants, l’évolution et le vieillissement cellulaire.

Doctorat en biologie. L’étudiante Autumn Peterson, auteur principal de l’étude, examine les cellules de levure avec le chercheur Anthony Burnetti, auteur correspondant de l’étude, dans le laboratoire. Crédit : Audra Davidson, Georgia Institute of Technology
À la recherche d’un regain d’énergie
La recherche a été inspirée par les travaux antérieurs du groupe sur l’évolution de la vie multicellulaire. Le groupe a publié son premier rapport sur son expérience d’évolution à long terme sur la multicellularité (MuLTEE) dans Nature L’année dernière, ils ont découvert comment leur organisme modèle unicellulaire, la « levure flocon de neige », était capable de développer une multicellularité sur 3 000 générations.
Tout au long de ces expériences d’évolution, une limitation majeure à l’évolution multicellulaire est apparue : l’énergie.
« L’oxygène a du mal à se diffuser profondément dans les tissus, et vous obtenez des tissus sans possibilité d’obtenir de l’énergie », explique Burnetti. « Je cherchais des moyens de contourner cette limitation énergétique basée sur l’oxygène. »
La lumière est une façon de donner aux organismes un regain d’énergie sans utiliser d’oxygène. Cependant, la capacité de transformer la lumière en énergie utilisable peut être compliquée d’un point de vue évolutif. Par exemple, la machinerie moléculaire qui permet aux plantes d’utiliser la lumière pour produire de l’énergie implique une multitude de gènes et de protéines difficiles à synthétiser et à transférer à d’autres organismes, à la fois en laboratoire et naturellement au cours de l’évolution.
Heureusement, les plantes ne sont pas les seuls organismes capables de convertir la lumière en énergie.
Faire simple
Les rhodopsines constituent un moyen plus simple pour les organismes d’utiliser la lumière : des protéines qui peuvent convertir la lumière en énergie sans machinerie cellulaire supplémentaire.
« Les rhodopsines se trouvent partout dans l’arbre de vie et sont apparemment acquises par des organismes obtenant des gènes les uns des autres au cours de l’évolution », explique Autumn Peterson, docteur en biologie. étudiant travaillant avec Ratcliff et auteur principal de l’étude.
Ce type d’échange génétique est appelé transfert horizontal de gènes et implique le partage d’informations génétiques entre des organismes qui ne sont pas étroitement liés. Le transfert horizontal de gènes peut provoquer des sauts évolutifs apparemment importants en peu de temps, comme la façon dont les bactéries sont rapidement capables de développer une résistance à certains antibiotiques. Cela peut se produire avec toutes sortes d’informations génétiques et est particulièrement fréquent avec les protéines rhodopsine.

Les chercheurs en biologie de Georgia Tech qui ont travaillé sur l’étude comprennent (de gauche à droite) le professeur adjoint de l’École des sciences biologiques William Ratcliff, la rédactrice de la subvention du Centre pour la dynamique microbienne et les infections Carina Baskett, docteur en biologie. l’étudiant Autumn Peterson (auteur principal) et le chercheur Anthony Burnetti (auteur correspondant). Crédit : Audra Davidson, Georgia Institute of Technology
« En cherchant un moyen d’introduire les rhodopsines dans des levures multicellulaires », explique Burnetti, « nous avons découvert que nous pouvions en apprendre davantage sur le transfert horizontal de rhodopsines qui s’est produit au cours de l’évolution dans le passé en les transférant dans des levures unicellulaires régulières. la levure là où elle n’a jamais été auparavant.
Pour voir s’ils pouvaient équiper un organisme unicellulaire de rhodopsine alimentée par l’énergie solaire, les chercheurs ont ajouté un gène de rhodopsine synthétisé à partir d’un champignon parasite à la levure de boulanger commune. Ce gène spécifique est codé pour une forme de rhodopsine qui serait insérée dans la vacuole de la cellule, une partie de la cellule qui, comme les mitochondries, peut transformer les gradients chimiques produits par des protéines comme la rhodopsine en énergie.
Équipée de rhodopsine vacuolaire, la levure se développe environ 2 % plus rapidement lorsqu’elle est allumée – un énorme avantage en termes d’évolution.
« Ici, nous avons un seul gène, et nous le transférons simplement à travers les contextes dans une lignée qui n’a jamais été phototrophe auparavant, et cela fonctionne », explique Burnetti. « Cela montre qu’il est vraiment aussi simple pour ce type de système, du moins parfois, de faire son travail dans un nouvel organisme. »
Cette simplicité fournit des informations clés sur l’évolution et en dit long sur « la facilité avec laquelle les rhodopsines ont pu se propager à travers tant de lignées et pourquoi cela peut être le cas », explique Peterson, qui a récemment reçu un prix du Howard Hughes Medical Institute (HHMI) Gilliam. Bourse pour son travail. Carina Baskett, rédactrice de subventions pour le Center for Microbial Dynamics and Infection de Georgia Tech, a également travaillé sur l’étude.
Parce que la fonction vacuolaire peut contribuer au vieillissement cellulaire, le groupe a également initié des collaborations pour étudier comment les rhodopsines pourraient réduire les effets du vieillissement chez la levure. D’autres chercheurs commencent déjà à utiliser une nouvelle levure similaire, alimentée par l’énergie solaire, pour étudier les progrès de la bioproduction, ce qui pourrait marquer de grandes améliorations dans des domaines tels que la synthèse de biocarburants.
Ratcliff et son groupe, cependant, souhaitent surtout explorer comment cet avantage supplémentaire pourrait avoir un impact sur le parcours de la levure unicellulaire vers un organisme multicellulaire.
« Nous avons ce magnifique système modèle de multicellularité simple », déclare Burnetti, faisant référence au système de longue date Expérience d’évolution à long terme de la multicellularité (MuLTEE). « Nous voulons lui donner une phototrophie et voir comment il change son évolution. »
L’étude a été financée par la National Science Foundation et la Fondation David et Lucile Packard.