Des scientifiques de Stanford ont synthétisé une forme rare d’or, Au2+, stabilisée par de la pérovskite halogénure, avec des applications potentielles dans les secteurs de l’électronique et de l’énergie, reliant leurs découvertes aux recherches antérieures du lauréat du prix Nobel Linus Pauling.
Une forme d’or qui n’est pas présente de manière stable dans la nature est au cœur d’un nouveau matériau cristallin aux propriétés intrigantes.
Pour la première fois, des chercheurs de Stanford ont trouvé un moyen de créer et de stabiliser une forme d’or extrêmement rare qui a perdu deux électrons chargés négativement, notés Au.2+. Le matériau stabilisant cette version insaisissable de l’élément précieux est une pérovskite halogénure, une classe de matériaux cristallins très prometteurs pour diverses applications, notamment des cellules solaires, des sources de lumière et des composants électroniques plus efficaces.
Étonnamment, l’Au2+ la pérovskite est également rapide et simple à préparer en utilisant des ingrédients du commerce à température ambiante.
« Ce fut une véritable surprise que nous ayons pu synthétiser un matériau stable contenant de l’Au2+« Je n’y croyais même pas au début », a déclaré Hemamala Karunadasa, professeur agrégé de chimie à la Stanford School of Humanities and Sciences et auteur principal de l’étude publiée récemment dans Chimie naturelle. «Créer ce premier Au2+ la pérovskite est passionnante. Les atomes d’or de la pérovskite présentent de fortes similitudes avec les atomes de cuivre des supraconducteurs à haute température et avec les atomes lourds dotés d’électrons non appariés, comme l’Au.2+montrent des effets magnétiques froids que l’on ne voit pas dans les atomes plus légers.
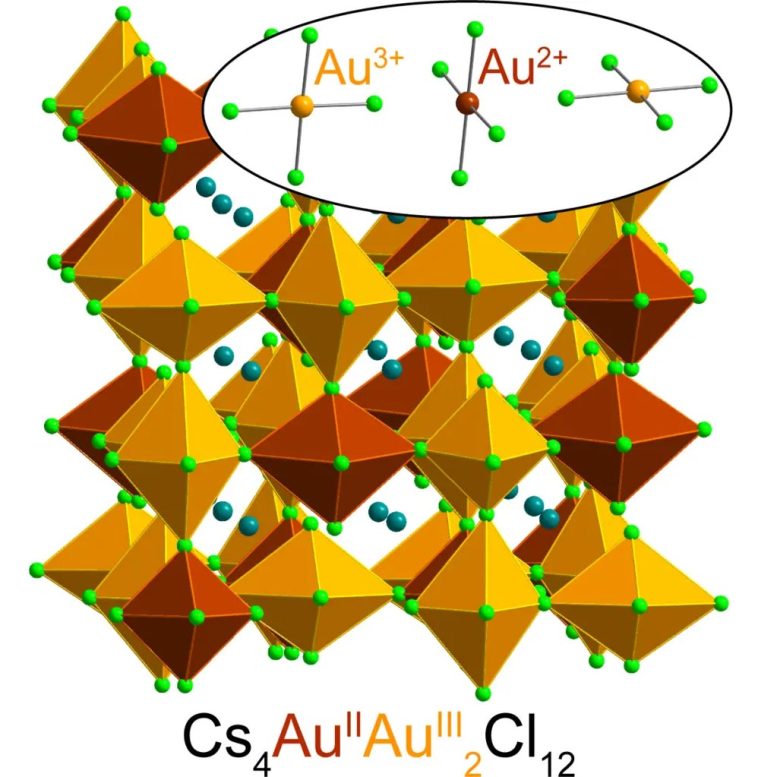
Structure de la pérovskite aux halogénures d’or. Les octaèdres allongés de chlorure d’or, composés d’or (Au) entourés de six atomes de chlore (Cl) voisins, sont ombrés dans la structure : les octaèdres rouge brûlé représentent le chlorure Au2+ et les octaèdres d’or représentent le chlorure Au3+. Les sphères turquoise représentent les atomes de césium (Cs) et les sphères vert clair représentent les atomes de chlore (Cl). L’encadré montre les liaisons or-chlorure les plus courtes. Crédit Karunadasa et al. 2023.
« Les pérovskites aux halogénures possèdent des propriétés vraiment attrayantes pour de nombreuses applications quotidiennes, nous cherchons donc à élargir cette famille de matériaux », a déclaré Kurt Lindquist, l’auteur principal de l’étude qui a mené la recherche en tant qu’étudiant au doctorat à Stanford et est maintenant postdoctorant. chercheur en chimie inorganique à université de Princeton. « Une Au sans précédent2+ la pérovskite pourrait ouvrir de nouvelles voies intrigantes.
Électrons lourds dans l’or
En tant que métal élémentaire, l’or a longtemps été apprécié pour sa relative rareté ainsi que pour sa malléabilité et son inertie chimique inégalées, ce qui signifie qu’il peut être facilement transformé en bijoux et en pièces de monnaie qui ne réagissent pas avec les produits chimiques présents dans l’environnement et ne ternissent pas avec le temps. Une autre raison clé de sa valeur est la couleur homonyme de l’or ; sans doute aucun autre métal à l’état pur n’a une teinte aussi riche.
La physique fondamentale derrière l’apparence acclamée de l’or explique également pourquoi Au2+ est si rare, a expliqué Karunadasa.
La raison fondamentale réside dans les effets relativistes, postulés à l’origine dans la célèbre théorie de la relativité d’Albert Einstein. « Einstein nous a appris que lorsque les objets se déplacent très rapidement et que leur vitesse approche une fraction significative de la vitesse de la lumière, les objets deviennent plus lourds », a déclaré Karunadasa.
Ce phénomène s’applique également aux particules et a de profondes conséquences pour les éléments lourds « massifs », comme l’or, dont les noyaux atomiques contiennent un grand nombre de protons. Ces particules exercent collectivement une immense charge positive, forçant les électrons chargés négativement à tourbillonner autour du noyau à des vitesses vertigineuses. En conséquence, les électrons deviennent lourds et entourent étroitement le noyau, atténuant sa charge et permettant aux électrons externes de dériver plus loin que dans les métaux classiques. Ce réarrangement des électrons et de leurs niveaux d’énergie conduit à ce que l’or absorbe la lumière bleue et apparaisse donc jaune à nos yeux.
En raison de la disposition des électrons de l’or, grâce à la relativité, le atome se produit naturellement sous forme d’Au1+ et Au3+perdant respectivement un ou trois électrons et rejetant Au2+. (Le « 2+ » indique une charge positive nette résultant de la perte de deux électrons chargés négativement, et le symbole chimique « Au » pour l’or vient de « aurum », le mot latin pour l’or.)
Une pincée de vitamine C
Avec juste la bonne configuration moléculaire, Au2+ peut durer, ont découvert les chercheurs de Stanford. Lindquist a déclaré qu’il était « tombé sur » le nouveau Au2+-héberger de la pérovskite tout en travaillant sur un projet plus large centré sur le magnétique semi-conducteurs pour une utilisation dans les appareils électroniques.
Lindquist a mélangé un sel appelé chlorure de césium et Au3+-chlorure ensemble dans l’eau et chlorhydrique ajouté acide à la solution « avec un peu de vitamine C ajoutée », a-t-il déclaré. Dans la réaction qui s’ensuit, la vitamine C (un acide) donne un électron (chargé négativement) à l’Au commun.3+ formant Au2+. Curieusement, Au2+ est stable dans la pérovskite solide mais pas en solution.
« En laboratoire, nous pouvons fabriquer ce matériau en utilisant des ingrédients très simples en cinq minutes environ à température ambiante », a déclaré Lindquist. « On se retrouve avec une poudre vert très foncé, presque noire, étonnamment lourde en raison de l’or qu’elle contient. »
Reconnaissant qu’ils pourraient avoir touché un nouveau but en matière de chimie, pour ainsi dire, Lindquist a effectué de nombreux tests sur la pérovskite, notamment la spectroscopie et la diffraction des rayons X, pour étudier comment elle absorbe la lumière et caractériser sa structure cristalline. Les groupes de recherche de Stanford en physique et chimie dirigés par Young Lee, professeur de physique appliquée et de photon science, et Edward Solomon, professeur de chimie Monroe E. Spaght et professeur de science des photons, ont également contribué à l’étude du comportement de Au2+.
Les expériences ont finalement confirmé la présence d’Au2+ dans une pérovskite et, ce faisant, a ajouté un chapitre à une histoire centenaire de chimie et de physique impliquant Linus Pauling, qui a reçu le prix Nobel de chimie en 1954 et le prix Nobel de la paix en 1962. Au début de sa carrière, il a travaillé sur des pérovskites d’or contenant les formes communes Au1+ et Au3+. Par coïncidence, Pauling a également étudié plus tard la structure de la vitamine C, l’un des ingrédients nécessaires pour produire une pérovskite stable contenant l’insaisissable Au.2+.
« Nous aimons le lien qui existe entre Linus Pauling et notre travail », a déclaré Karunadasa. « La synthèse de cette pérovskite constitue une bonne histoire. »
Pour l’avenir, Karunadasa, Lindquist et leurs collègues prévoient d’étudier davantage le nouveau matériau et de peaufiner sa chimie. L’espoir est qu’un Au2+ la pérovskite peut être utilisée dans des applications qui nécessitent du magnétisme et de la conductivité lorsque les électrons sautent de l’Au2+ à Au3+ dans la pérovskite.
«Nous sommes ravis d’explorer ce qu’est un Au2+ la pérovskite pourrait faire l’affaire », a déclaré Karunadasa.
Karunadasa est aussi un chercheur principal au Institut Précourt pour l’énergie et chercheur principal et chercheur universitaire à l’Institut des sciences des matériaux et de l’énergie de Stanford, Laboratoire national des accélérateurs du SLAC. Solomon est professeur de science des photons à la source lumineuse de rayonnement synchrotron de Stanford, SLAC. Les co-auteurs supplémentaires de Stanford sont Christina R. Deschene et Alexander J. Heyer, étudiants diplômés du Département de chimie ; et Jiajia Wen, scientifique au SLAC. Les autres co-auteurs incluent Armin Eghdami et Alexander G. Smith, étudiants diplômés du Département de physique de l’Université de Californie à Berkeley, et Jeffrey B. Neaton, professeur de physique à l’Université de Californie à Berkeley ; et Dominic H. Ryan, professeur de physique à l’Université McGill.
La recherche a été financée en partie par la National Science Foundation des États-Unis, le Département américain de l’Énergie, le Fonds de recherche du Québec – Nature et technologies et le Conseil de recherches en sciences naturelles et en génie du Canada.




