Les méthodes traditionnelles de développement de médicaments impliquent l'identification d'une protéine cible (par exemple, un récepteur des cellules cancéreuses) qui provoque une maladie, puis de rechercher d'innombrables candidats moléculaires (médicaments potentiels) qui pourraient se lier à cette protéine et bloquer sa fonction. Ce processus est coûteux, prend du temps et a un faible taux de réussite.
Les chercheurs kaist ont développé un modèle d'IA qui, en utilisant uniquement des informations sur la protéine cible, peut concevoir des candidats à des médicaments optimaux sans données moléculaires antérieures, ce qui a augmenté de nouvelles possibilités de découverte de médicaments. La recherche est publiée dans la revue Science avancée.
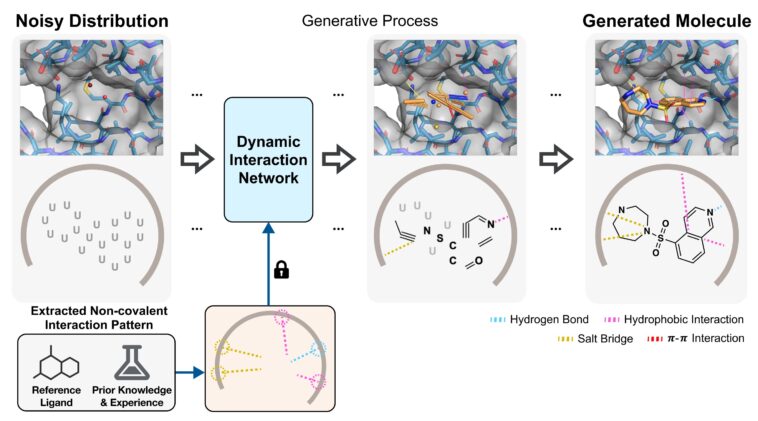
L'équipe de recherche dirigée par le professeur Woo Youn Kim au Département de chimie a développé un modèle d'IA nommé Bind (modèle de diffusion de liaison et d'interaction), qui peut concevoir et optimiser les molécules de candidats médicamenteuses adaptées à la structure d'une protéine seule, sans avoir besoin d'informations antérieures sur les molécules de liaison. Le modèle prédit également le mécanisme de liaison (interactions non covalentes) entre le médicament et la protéine cible.
L'innovation principale de cette technologie réside dans son approche de « conception simultanée ». Les modèles AI précédents se sont concentrés sur la génération de molécules ou à évaluer séparément si la molécule générée pouvait se lier à la protéine cible. En revanche, ce nouveau modèle considère le mécanisme de liaison entre la molécule et la protéine pendant le processus de génération, permettant une conception complète en une seule étape.
Puisqu'il prépare les facteurs critiques dans la liaison des protéines-ligands, il a une probabilité beaucoup plus élevée de générer des molécules efficaces et stables. Le processus de génération montre visuellement comment les types et les positions des atomes, des liaisons covalentes et des interactions sont créés simultanément pour s'adapter au site de liaison de la protéine.
De plus, ce modèle est conçu pour répondre simultanément à plusieurs critères de conception de médicaments essentiels, tels que l'affinité de liaison cible, les propriétés de type médicament et la stabilité structurelle. Les modèles traditionnels ont souvent optimisé pour un ou deux buts au détriment des autres, mais ce nouveau modèle équilibre divers objectifs, améliorant considérablement son applicabilité pratique.
L'équipe de recherche a expliqué que l'IA fonctionne sur la base d'un «modèle de diffusion» – une approche générative où une structure devient de plus en plus raffinée à partir d'un état aléatoire. Il s'agit du même type de modèle utilisé dans Alphafold 3, l'outil lauréat du prix Nobel Chemistry 2024 pour la génération de structure protéine-ligand, qui a déjà démontré une grande efficacité.
Contrairement à Alphafold 3, qui fournit des coordonnées spatiales pour les positions des atomes, cette étude a introduit un guide basé sur les connaissances fondée sur des lois chimiques réelles, telles que les longueurs de liaison et les distances protéine-ligand – permettant une génération de structure chimiquement réaliste.
De plus, l'équipe a appliqué une stratégie d'optimisation où des modèles de liaison exceptionnels à partir de résultats antérieurs sont réutilisés. Cela a permis au modèle de générer encore de meilleurs candidats en médicaments sans formation supplémentaire. Notamment, l'IA a produit avec succès des molécules qui se lient sélectivement aux résidus mutés de l'EGFR, une protéine cible liée au cancer.
Cette étude est également significative car elle progresse au-delà des recherches antérieures de l'équipe, ce qui nécessitait une entrée préalable sur les conditions moléculaires pour le modèle d'interaction de la liaison aux protéines.
Le professeur Woo Youn Kim a déclaré: «L'IA nouvellement développée peut apprendre et comprendre les caractéristiques clés requises pour une forte liaison à une protéine cible et concevoir des molécules optimales de médicament, même sans aucune contribution préalable. Cela pourrait changer considérablement le paradigme du développement de médicaments.
« Étant donné que cette technologie génère des structures moléculaires en fonction des principes des interactions chimiques, il devrait permettre un développement de médicaments plus rapide et plus fiable. »