L'azote rejoint enfin le niveau d'élite d'éléments comme le carbone qui peuvent former des allotropes neutres – des formes structurelles diffeuges d'un seul élément chimique. Des chercheurs de l'Université de Justus Liebig, Giessen, Allemagne, ont synthétisé l'hexanitrogène neutre (N6) – le premier allotrope neutre de l'azote depuis la découverte du dinitrogen naturel (n2) Au XVIIIe siècle, qui est cryogéniquement stable et peut être préparé à température ambiante.
Cette nouvelle étude, publiée dans Nature, hexanitroge synthétisé (n6) par réaction en phase gazeuse, les ingrédients principaux étant le chlore (Cl2) ou brome (br2) et un azide d'argent solide extrêmement réactif et explosif (AGN3), sous une pression réduite.
Les chercheurs ont répandu AGN3 sur la surface intérieure, et un halogène gazeux (Cl2 ou br2) a été passé à travers le solide sous une pression réduite à température ambiante. La réaction déclenchée par le processus produit n6 aux côtés des sous-produits du chloronitrène (CLN) et de l'acide hydrazoïque (HN3).
Ces molécules ont ensuite été piégées dans des matrices d'argon – une matrice inerte de l'argon solide – à des conditions cryogéniques (10 Kelvin) pour stabiliser et isoler le n hautement réactif6.
Les formes moléculaires d'azote sont très prometteuses en tant que matériaux neutres et à haute énergie en carbone. En décomposition, ils libèrent une grande quantité d'énergie alors qu'ils se décomposent en leur n stable2 forme, un gaz inerte non toxique, contrairement aux carburants conventionnels qui produisent des gaz à effet de serre tels que le CO2.
Malheureusement, n2 est la seule allotrope naturelle (forme moléculaire) d'azote, qui, en raison de sa nature inerte provenant de liaisons triples exceptionnellement fortes, est inadaptée à une utilisation comme carburant.

Pendant des décennies, les scientifiques ont essayé de synthétiser des molécules d'azote neutres plus grandes en tant que matériaux d'énergie mais ont échoué en raison de la nature extrêmement instable des molécules de polylitrogène.
Des études antérieures ont détecté le radical azide (-n3) et le deuxième n4 via la spectroscopie, mais leur structure est restée un mystère. Sur le front théorique, les structures de n4 à n12 ont été prédits, mais aucun n'a été isolé expérimentalement, car ils sont considérés comme trop instables.
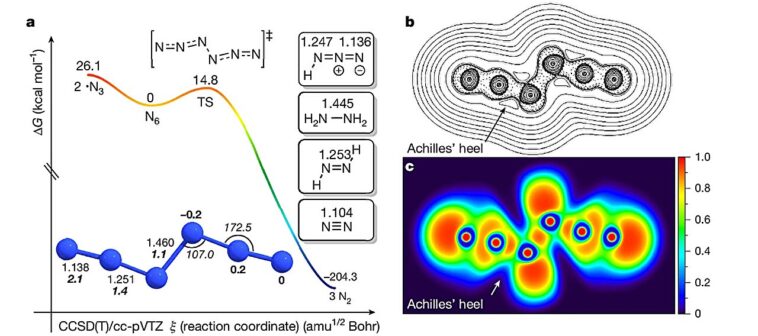
Cette étude a cassé la tendance non seulement en synthétisant avec succès le N neutre6 molécule mais identifiant également sa structure acyclique linéaire avec c2h symétrie. La molécule se compose d'une chaîne de six atomes d'azote où deux azides (n3) Les unités et trois atomes d'azote sont maintenus ensemble par des liaisons doubles rejoints par une seule liaison N – N au centre.
Le mécanisme impliquait probablement une réaction en phase gazeuse en deux étapes. Au début, le Cl gazeux2 ou br2 réagi avec de l'azide argenté pour produire des halogénures en argent (Agx, où x = cl ou br) et azide halogène (xn3). L'azide halogène formé au premier pas a réagi avec une autre molécule d'azide d'argent pour produire des halogénures d'argent et de l'hexanitrogène (n6).

Alors6 Produit à température ambiante est resté stable à des températures cryogéniques, permettant aux chercheurs de l'isoler comme un film pur à 77 K – la température à laquelle l'azote devient liquide. Les calculs de calcul ont révélé que la molécule avait une demi-vie de 35,7 millisecondes à température ambiante et plus de 132 ans dans des conditions cryogéniques.
Les chercheurs ont également découvert que n6lors de la décomposition, libère une quantité exceptionnelle d'énergie – 2,2 fois plus par masse unitaire que le TNT explosif connu et deux fois celui de RDX.
Ils soulignent que la préparation d'un allotrope à l'azote moléculaire métastable au-delà de N2 Avance non seulement la compréhension scientifique fondamentale, mais a également un potentiel pour les futures applications de stockage d'énergie.
Écrit pour vous par notre auteur Sanjukta Mondal, édité par Sadie Harley, et vérifié et examiné par Robert Egan – cet article est le résultat d'un travail humain minutieux. Nous comptons sur des lecteurs comme vous pour garder le journalisme scientifique indépendant en vie. Si ce rapport vous importe, veuillez considérer un don (surtout mensuel). Vous obtiendrez un sans publicité compte comme un remerciement.