Les chercheurs ont fait des progrès significatifs dans la compréhension de la formation des synapses. Ils ont utilisé la technologie CRISPR pour observer le développement des vésicules synaptiques et ont découvert que les composants synaptiques partagent une voie de transport commune. Cette découverte, associée à la découverte d’organites de transport neuronaux uniques, offre de nouvelles perspectives sur les fonctions neuronales et des approches thérapeutiques potentielles pour les dommages neurologiques.
Que ce soit dans le cerveau ou dans les muscles, les synapses sont présentes partout où existent des cellules nerveuses. Les synapses, les connexions entre les neurones, sont fondamentales dans le processus de transmission de l’excitation, qui est essentiellement la communication entre les neurones. Comme dans tout processus de communication, il existe un émetteur et un récepteur : les processus des cellules nerveuses appelés axones génèrent et transmettent des signaux électriques, agissant ainsi comme émetteurs de signaux.
Les synapses sont des points de contact entre les terminaisons nerveuses axonales (lessynapse) et les neurones post-synaptiques. Au niveau de ces synapses, l’impulsion électrique est convertie en messagers chimiques qui sont reçus et détectés par les post-synapses du neurone voisin. Les messagers sont libérés à partir de sacs membranaires spéciaux appelés vésicules synaptiques.
En plus de transmettre des informations, les synapses peuvent également stocker des informations. Bien que la structure et la fonction des synapses soient relativement bien comprises, on sait peu de choses sur la façon dont elles se forment.
Une équipe du Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP) à Berlin a désormais apporté un éclairage significatif sur ce mystère. Des scientifiques de la Charité-Universitätsmedizin, du Centre Max Delbrück de médecine moléculaire (MDC) et des universités de Leipzig, Chicago et Sheffield ont également contribué à ce travail remarquable.
La protéine fluorescente révèle le développement de vésicules synaptiques
Pour suivre la formation des pré-synapses depuis le début, les chercheurs ont utilisé des ciseaux génétiques CRISPR pour insérer une protéine fluorescente dans les cellules souches humaines et ont généré des neurones à partir des cellules souches modifiées. Grâce au marqueur fluorescent, les chercheurs ont désormais pu observer le développement de vésicules synaptiques naissantes dans des cellules nerveuses humaines vivantes en développement directement au microscope.
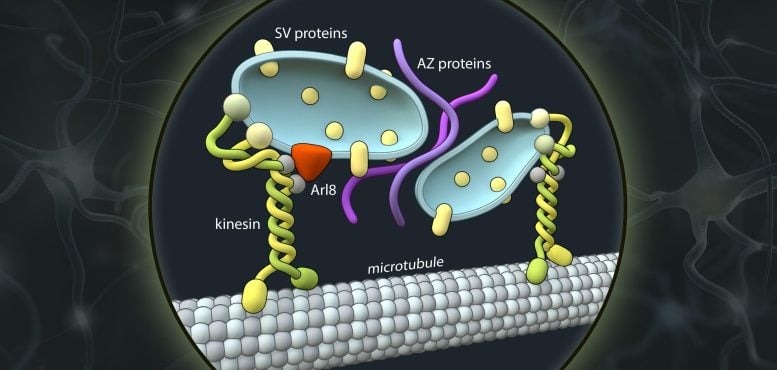
Représentation schématique des vésicules de transport axonal (bleu) transportant des protéines présynaptiques (protéines SV et AZ). Les protéines motrices kinésine (KIF1A) fixent ces vésicules et les transportent le long des axones jusqu’au site de formation des synapses. Crédit : Barth van Rossum
Les vésicules synaptiques sont des vésicules membranaires qui contiennent des messagers et sont stockées au niveau de chaque synapse pour convertir les signaux électriques en signaux chimiques. Avec les protéines d’échafaudage qui indiquent aux vésicules synaptiques où se trouve la synapse et les canaux calciques qui traduisent chimiquement le signal électrique, ces vésicules forment les éléments centraux de la pré-synapse.
Les trois composants possèdent leurs propres gènes et sont donc constitués de molécules protéiques différentes. Pour cette raison, on pensait auparavant qu’ils empruntaient également des chemins différents pour finalement se réunir en un seul endroit pour former une synapse fonctionnelle.
Tous les composants partent ensemble
Cependant, les observations des chercheurs vont à l’encontre de cette hypothèse. « Les protéines des vésicules synaptiques et les protéines de la « zone active » et probablement aussi les protéines d’adhésion qui maintiennent les synapses ensemble, partagent le même bus », déclare le professeur Dr. Volker Haucke, chef du groupe de recherche, décrivant cette découverte surprenante. «C’était très controversé. Et pourtant, nos données sur les neurones humains en culture semblent assez claires.
Mais comment exactement les protéines parviennent-elles au site de formation des synapses ? Dans leur étude, les chercheurs ont pu montrer, entre autres, qu’une machinerie de protéines motrices alimente le transport axonal. Selon leurs conclusions, le principal moteur est une kinésine connue sous le nom de « KIF1A ». Cette protéine motrice est surtout connue pour son association avec des troubles neurologiques du système nerveux périphérique et du cerveau. « Nous soupçonnons que les mutations de KIF1A interfèrent avec le transport axonal des protéines pré-synaptiques, entraînant des symptômes neurologiques tels que des troubles du mouvement, une ataxie ou un handicap mental », explique Volker Haucke. Le scientifique est également professeur de pharmacologie moléculaire à la Freie Universität Berlin.
De plus, les chercheurs ont également pu déterminer l’identité biologique cellulaire des porteurs axonaux. Cela a conduit à une autre surprise : alors que la grande majorité des vésicules sécrétoires proviennent de ce qu’on appelle l’appareil de Golgi, les vésicules de transport axonal ne contiennent pas de marqueurs de Golgi, mais partagent des marqueurs avec le système endolysosomal, qui est généralement impliqué dans la dégradation des protéines défectueuses. dans les cellules non neuronales. Il s’agissait d’une nouvelle combinaison de microscopie optique et électronique à haute résolution qui a permis aux chercheurs de visualiser de manière ultrastructurale les vésicules de transport axonal, leur permettant ainsi de décrire leur taille et leur forme.
Découverte d’organites de transport qui n’existent que dans les neurones
« Nos travaux suggèrent que les neurones ont inventé un nouveau type d’organite, un organite de transport qui pourrait être propre aux neurones », a expliqué la Dre Sila Rizalar, chercheuse postdoctorale au FMP et auteure principale de l’étude publiée dans Science. « C’était aussi peu connu que le mode de transport partagé. »
Les nouveaux résultats de la recherche fondamentale pourraient un jour être utiles à des applications cliniques. Après tout, lorsque les points de contact entre les neurones tombent en panne, que ce soit en raison d’une maladie, d’un accident ou du processus de vieillissement, il est important de comprendre le mécanisme du transport axonal et les protéines clés impliquées afin d’intervenir thérapeutiquement. « Idéalement, il serait possible de restaurer ou d’améliorer le transport axonal pour favoriser la régénération neuronale ou lutter contre le vieillissement », remarque Volker Haucke.
Bien que les chercheurs aient désormais découvert un mécanisme clé de la formation des synapses, de nombreuses questions restent sans réponse, telles que la formation des organites de transport récemment découverts, de quoi ils sont constitués et comment ils livrent leur cargaison – les molécules synaptiques – à leur destination. Cela soulève également la question de savoir si, peut-être, les souvenirs permanents sont stockés en utilisant le même mécanisme de transport axonal que celui utilisé pour former les synapses. Autant de questions auxquelles Volker Haucke et son équipe souhaitent désormais répondre. Les perspectives sont passionnantes.