Les mitochondries sont des organites cellulaires qui jouent un rôle important dans la fabrication de l'ATP (adénosine triphosphate), le carburant moléculaire qui alimente la plupart des fonctions cellulaires. Ces organites sont à l'origine il y a plus d'un milliard d'années lorsqu'une cellule archéale primitive est entrée dans une relation symbiotique avec une bactérie ancestrale. Au fil du temps, les mitochondries sont devenues essentielles pour le métabolisme et la production d'énergie, tout en transférant la plupart de leurs gènes à l'hôte. En conséquence, ils comptent désormais sur la cellule hôte pour fournir la plupart de leurs protéines, qui sont synthétisées par des ribosomes à l'extérieur de l'organelle et doivent être correctement délivrées aux mitochondries.
Maintenant, les scientifiques de Caltech ont découvert de nouveaux détails sur la façon dont les protéines mitochondriales sont délivrées des ribosomes dans le cytosol, le liquide autour du noyau, aux mitochondries. Dans une tournure surprenante, le processus est largement façonné par les détails techniques du repliement des protéines.
« Il s'avère que la localisation des protéines en mitochondries implique une voie complexe multicouche qui est câblée autour des principes biophysiques du repliement des protéines », explique Shu-ou Shan, professeur de chimie altair à Caltech.
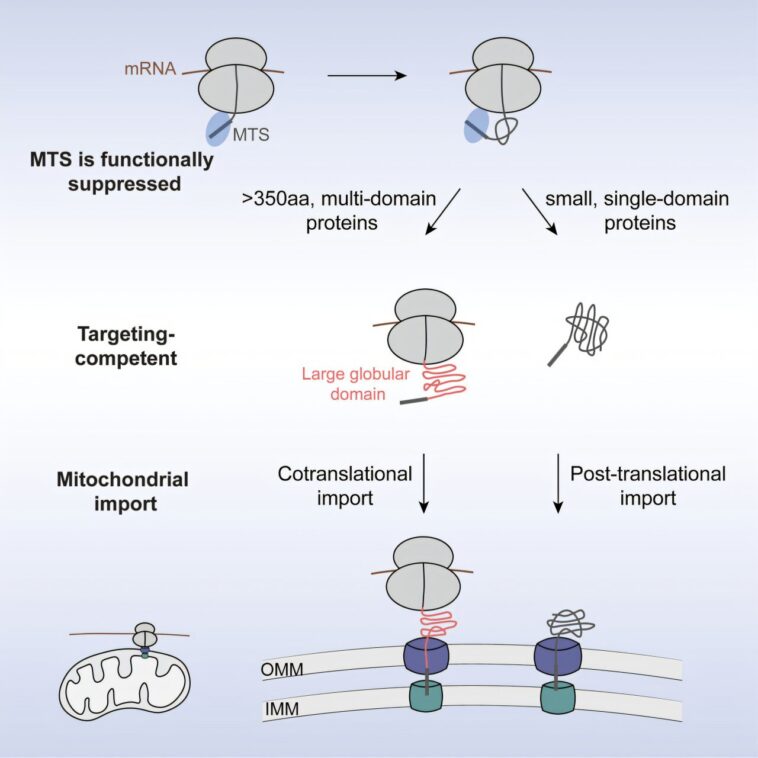
Pendant des décennies, le modèle dominant de la biochimie a soutenu que les protéines mitochondriales sont importées uniquement après la synthèse des protéines, ou traduction, se termine complètement. (Ce processus axé sur les ribosomes consiste à ajouter des acides aminés un par un à une chaîne en croissance, après la séquence présentée par le code génétique de la cellule.) Dans un nouvel article qui apparaît dans le journal CelluleShan et ses collègues offrent une révision à ce modèle, montrant que jusqu'à 20% des protéines mitochondriales peuvent être importées cotranslationnellement, ce qui signifie qu'elles entrent dans les mitochondries pendant la traduction lorsque les protéines sont encore en train d'être synthétisées par le ribosome.
« Une fois que nous avons identifié ces protéines mitochondriales qui sont importées cotranslationnellement, nous avons demandé: » Quelle est la particularité de ce sous-ensemble de protéines? « », A déclaré Zikun Zhu (Ph.D. '24), ancien étudiant diplômé de Shan et auteur principal de l'article.
Il s'avère que la caractéristique la plus importante de ces protéines est que ce sont de grandes molécules qui se replient de manière complexe. Ces protéines topologiquement complexes sont riches en résidus – les acides aminés dans la chaîne qui constituent la protéine – qui, bien que distants les uns des autres en séquence linéaire, doivent se lier ensemble pour que la protéine se replie dans la structure tridimensionnelle appropriée. « Cela devient un processus beaucoup plus difficile que de simplement replier les interactions entre les résidus voisins », explique Shan.
En conséquence, le système d'importation cotranslationnelle dans les mitochondries hiérarte ces protéines vraiment difficiles à replier. Cela est logique si vous considérez que les grandes structures doivent éventuellement passer par des canaux étroits sur la membrane mitochondriale pendant l'importation. « Il y aura un problème si vous laissez ces grandes protéines très complexes terminer la traduction dans le cytosol », explique Shan. « Ils resteront coincés dans des structures irréversibles, puis vous ne bloquerez pas seulement l'importation, vous obtiendrez tous les canaux. »
Mais comment la cellule sait-elle quelles protéines doivent être importées pendant la traduction?
L'équipe a constaté que presque toutes ces protéines transportent une séquence de ciblage mitochondriale, qui est un signal qui dirige les protéines vers les mitochondries. Pourtant, étonnamment, cela ne suffit pas à lui seul pour indiquer que ce sous-ensemble de protéines soit délivré pendant la traduction. ZHU a mené des expériences qui ont montré que le système attend un deuxième signal moléculaire pour déplacer tôt une protéine vers les mitochondries. Ce signal se présente sous la forme du premier grand domaine protéique, ou unité structurelle pliable dans la séquence, qui émerge du ribosome.
« C'est comme faire enfermer votre carte d'embarquement », explique Zhu. « La séquence de ciblage est la carte d'embarquement, mais pour y accéder, vous avez besoin du code pour ouvrir la valise. Dans ce cas, le grand domaine est ce code. »
Les scientifiques ont même été en mesure de transplanter des exemples de domaines de protéines aussi grands vers d'autres protéines mitochondriales qui sont normalement importées après la traduction et ont montré que les domaines servaient en effet de signaux transférables capables de réaffecter des protéines à importer pendant la traduction.
« Le ciblage cotranslationnel vers les mitochondries se révèle être complètement différent du ciblage à d'autres organites », explique Zhu. « À l'avenir, il sera passionnant de découvrir plus de détails mécanistes et, finalement, de manipuler le moment de l'importation de protéines mitochondriaux.
Le document est intitulé «Principes de l'importation de protéines mitochondriales cotranslationnelles». Les auteurs de Caltech supplémentaires sont Taylor A. Stevens (Ph.D. '24), un associé de recherche postdoctorale en biologie et génie biologique, et Rimming Huang, étudiant diplômé en biochimie et biophysique moléculaire. Saurav Mallik du Weizmann Institute of Science en Israël et Emmanuel D. Levy de l'Université de Genève en Suisse sont également des auteurs.