La recherche de l'Université Simon Fraser (SFU) donne de nouvelles perspectives sur l'une des propriétés les plus perplexes du collagène. Un papier dans Actes de l'Académie nationale des sciences Par le professeur de physique Nancy Ford et le chercheur postdoctoral Alaa al-Shaer décrit les caractéristiques moléculaires clés qui aident à permettre à cette protéine notoirement instable de maintenir sa structure.
Le collagène représente environ 20% de la protéine trouvée dans notre corps. Il assure la stabilité de nos tissus conjonctifs tels que le tendon, l'os, le cartilage et la peau, et forme un échafaudage dans lequel les cellules se développent et prospèrent.
C'est aussi une protéine qui a perplexe les scientifiques depuis longtemps. Comment une molécule qui est structurellement instable à la température corporelle peut-elle jouer un rôle si important en aidant à maintenir notre corps ensemble?
Comprendre cela peut être essentiel pour apprendre comment nous pouvons mieux traiter les maladies associées au collagène telles que les maladies osseuses fragiles, le syndrome d'Ehlers-Danlos et le diabète.
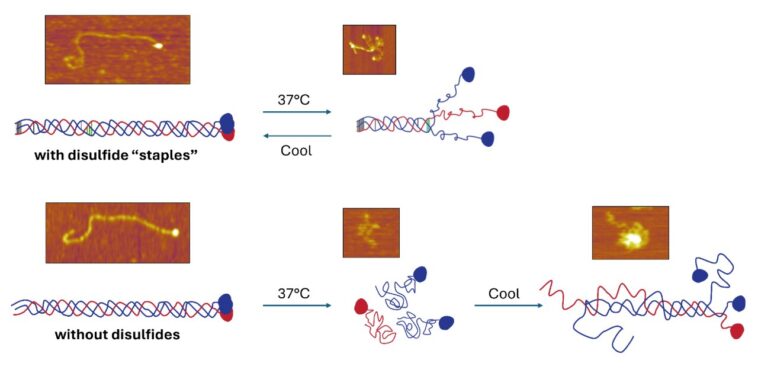
Les collagènes individuels sont trop petits pour être vus en utilisant des microscopes optiques conventionnels, donc Al-Shaer a utilisé une technique appelée microscopie à force atomique (AFM) pour capturer des images de protéines de collagène à différentes températures. Forde explique que cette technique permet aux chercheurs de « ressentir » des objets comme lire du braille ou une aiguille sur un disque.
Lorsqu'il est stable, le collagène a une structure à triple hélice avec trois brins tordus comme une corde ou un fil. À des températures plus élevées, ces fils se démêlent en bobines aléatoires. Al-Shaer a enregistré des centaines d'images pour cartographier ce processus de démêlage, et comment, dans certains cas, les protéines ont pu replier ensemble lorsqu'elles étaient refroidies.
Elle a constaté que les acides aminés présents dans le collagène IV appelées cystéines peuvent former des liaisons entre les brins individuels qui peuvent les « agracer » ensemble. Là où ces agrafes existent, le collagène IV a résisté à un démêlage lorsqu'il était chauffé et était plus susceptible de se réparer en se refroidissant. Les collagènes sans ces liaisons se sont effondrés plus facilement et n'ont pas été en mesure de remonter lorsqu'ils sont refroidis.
Lorsqu'elle a recherché des bases de données de séquences protéiques pour des cystéines similaires chez d'autres espèces, Al-Shaer a constaté que cet aliment de base chimique est très commun dans le collagène IV à partir d'autres formes de vie multicellulaires, y compris certaines espèces qui ont d'abord évolué il y a très longtemps.
« Cela indique que ces cystéines ont un rôle fonctionnel important », explique Forde, « car s'ils avaient muté à quelque chose d'autre et fait un tout aussi bon travail, nous nous attendons à voir d'autres acides aminés à ces postes. »
« Cette étude était la première fois que nous utilisons l'imagerie AFM pour étudier la stabilité du collagène à différentes températures et cartographier les voies de pliage et de dépliage. Nous pensons que cela est incroyablement prometteur pour répondre à de futures questions pour le domaine », explique Forde.
Forde note que de nombreuses études antérieures sur la stabilité du collagène ont utilisé de courtes volets de peptides synthétiques. « Il est difficile de savoir à quel point les leçons apprises dans ces petites études de peptide se traduisent en effets au sein des protéines de collagène pleine longueur, dont les séquences sont beaucoup plus complexes », dit-elle. L'AFM peut aider à vérifier ou à remettre en question ces résultats.
Forde note que plusieurs étudiants diplômés et de premier cycle ont aidé à faire progresser le travail de son laboratoire sur le collagène, et son équipe a hâte de développer davantage ces techniques pour répondre à de nombreuses autres questions.
« Nous aimerions examiner les collagènes mutés ou autrement modifiés chimiquement associés à la maladie et au vieillissement, afin de mieux comprendre le mécanisme de la maladie », dit-elle.
« Et je veux continuer à travailler avec des étudiants incroyables de la faculté des sciences de SFU pour faire ces découvertes. »