Une équipe de recherche a réussi à concevoir une nouvelle enzyme Hydrolase PET, PET2-21M, réalisant une amélioration remarquable de la biodégradation des plastiques de téréphtalate de polyéthylène (PET) de qualité de bouteille. Une activité élevée vers les mélanges textiles TEP / Cotton et TEP / Polyuréthane (PU) a également été démontrée séparément avec la variante étroitement apparentée PET2-14M-6HOT.
L'étude est publiée dans la revue ACS Chimie et ingénierie durable.
Cette percée importante traite du défi mondial urgent du recyclage des déchets pour animaux de compagnie en offrant une alternative durable et efficace aux processus de recyclage conventionnels.
PET est un polymère synthétique largement utilisé proéminent dans les bouteilles, les textiles et les matériaux d'emballage, représentant environ 83% du marché des fibres synthétiques. Malgré sa recyclabilité intrinsèque, les méthodes traditionnelles de recyclage mécanique entraînent fréquemment une dégradation de la qualité des matériaux et présentent une efficacité limitée pour les matériaux mélangés complexes tels que TEP / Cotton et PET / PU.
Le recyclage chimique, bien que capable de produire des matériaux de haute pureté, exige généralement des conditions difficiles et des réactifs dangereux pour l'environnement, limitant ainsi sa durabilité pratique.
En réponse, le recyclage enzymatique est devenu une alternative attrayante en raison de sa capacité à dépolymériser la TEP dans ses constituants monomères d'origine dans des conditions aqueuses plus douces.
Pour améliorer l'efficacité dégradant les animaux de compagnie de l'Enzyme Pet2, les chercheurs dirigés par le professeur Akihiko Nakamura de l'Institut de recherche des sciences et technologies vertes, Shizuoka University (également professeur à poitrine transversale à l'Institut pour les sciences moléculaires jusqu'à March 2025), en collaboration avec les chercheurs Takashi Matsuzaki et Toshiyuki SAKI SAKI DE KIRIN Ltd., le professeur Ryota Iino de l'Institut de sciences moléculaires, et le professeur Nobuyasu Koga de l'Institut de recherche sur les protéines, l'Université d'Osaka, ont adopté une vaste stratégie d'ingénierie.
Ils ont systématiquement utilisé une mutagenèse aléatoire et ciblée, combinant sept mutations bénéfiques nouvellement identifiées avec une variante modifiée PET2-7M précédemment rapportée, résultant en l'enzyme PET2-14M très active.
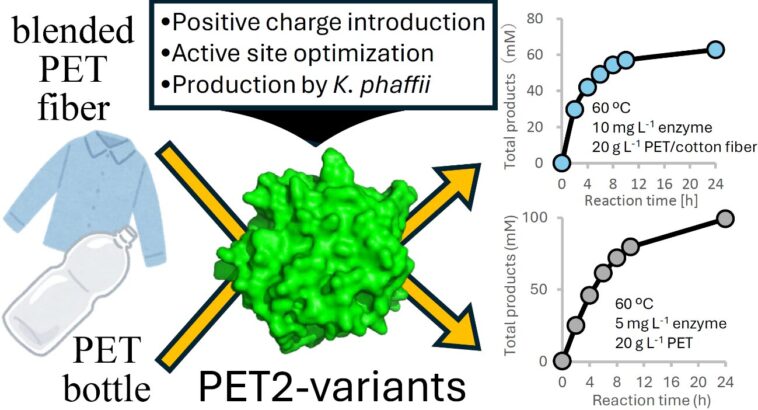
Des modifications de surface supplémentaires, qui ont introduit des charges positives pour améliorer la liaison du substrat et des altérations stratégiques de la fente de liaison au substrat basée sur une autre enzyme, la hotpetase, comme modèle structurel, a conduit à la création de PET2-14M-6HOT.
Une optimisation supplémentaire a produit la variante d'ingénierie finale PET2-21M. De plus, une production à grande échelle du PET2-14M-6HOT et PET2-21M a été réalisée chez l'hôte de levure, Komagataella Phaffii.
Notamment, PET2-14M-6HOT a atteint des rendements jusqu'à 691 mg L-1 Après 137 heures de culture, démontrant une efficacité d'expression élevée sans hétérogénéité induite par la glycosylation.
Le PET2-21M a démontré une activité catalytique significativement améliorée par rapport à l'enzyme d'origine PET2 de type sauvage, avec des tests initiaux à petite échelle révélant un produit total de produit environ 28,6 fois supérieur.
Les expériences de mise à l'échelle ultérieures dans des réacteurs de 300 ml ont en outre validé ces améliorations; Notamment, PET2-21M a dépolymérisé environ 95% de la poudre de compagnie de grade de bouteille commerciale (20 g L-1) Dans les 24 heures à 60 ° C, tandis que l'enzyme de référence LCC-ICCG a nécessité sa température optimale de 72 ° C pour atteindre une conversion comparable de 91%.
La supériorité de PET2-21M était particulièrement évidente dans des conditions de chargement enzymatiques réduites. Même lorsque la concentration enzymatique a été divisée en deux à 2,5 mg L-1PET2-21M a maintenu environ 50% d'efficacité de dégradation, doublant presque les performances du LCC-ICCG, qui n'a atteint que 26% de conversion dans des conditions identiques.
Cela met en évidence le potentiel substantiel de PET2-21M à réduire les exigences catalytiques et les coûts associés.
Surtout, PET2-21M a conservé son avantage concurrentiel dans des conditions de chargement de substrat plus élevées (40 g L-1). À une dose enzymatique de 10 mg L-1PET2-21M a atteint une conversion de 79% à 60 ° C, rivalisant étroitement à la conversion de 95% de LCC-ICCG à sa température optimale plus élevée (72 ° C).
De plus, en réduisant la dose enzymatique à 5 mg L-1PET2-21M a toujours surperformé le LCC-ICCG, démontrant une conversion de 44% contre 29% pour LCC-ICCG.
Cette performance robuste à des températures modérées et une réduction des ratios enzymatiques / sous-substrats positionne PET2-21m en tant que candidat très prometteur pour les processus de recyclage des animaux de compagnie industriels, ce qui permet potentiellement de réductions substantielles de la consommation d'énergie et des dépenses de catalyseur.
Pour évaluer le potentiel de recyclage des hydrolases PET modifiées pour les déchets textiles, le PET2-14M-6HOT a été comparé à l'enzyme de référence LCC-ICCG sur les fibres de PET pures et les mélanges textiles.
À 60 ° C, PET2-14M-6HOT a généré 75,7 mm de produits de dégradation totale à partir de fibres de TEP pures dans les 24 heures, ce qui représente une amélioration de 1,4 fois par rapport au LCC-ICCG testé à son 70 ° C optimal. De même, PET2-14M-6HOT a atteint une efficacité catalytique plus élevée sur les mélanges TEP / Cotton (65/35% en poids), produisant des produits de 62,8 mm contre 46,7 mm par LCC-ICCG, avec une interférence minimale à partir de fibres de coton.
Pour les mélanges textiles pour animaux de compagnie / PU difficiles (85/15% en poids), les deux enzymes présentaient une activité réduite au-dessus de la température de transition de verre de PU (tg ≈ 55 ° C).
Néanmoins, à une température de réaction plus faible de 50 ° C, PET2-14M-6HOT a maintenu une activité catalytique substantielle, produisant 19,2 mm de produits de dégradation – plus du double de 8,2 mm obtenus par LCC-ICCG dans des conditions identiques. Cela souligne la capacité supérieure de PET2-14M-6HOT pour le traitement des textiles mélangés complexes, qui ont traditionnellement résisté à la dégradation enzymatique.
Ces résultats confirment le potentiel significatif de la famille enzymatique PET2 pour le recyclage enzymatique à l'échelle industrielle. Leur capacité à dégrader efficacement divers flux de déchets pour animaux de compagnie, y compris des mélanges textiles difficiles à des températures modérées, prend en charge fortement des avantages plus larges d'applicabilité et de durabilité dans les processus de recyclage des animaux de compagnie.
Ces résultats représentent une avance substantielle vers la réalisation d'une économie circulaire plus durable et économiquement viable.
La capacité supérieure des enzymes PET2 d'ingénierie à dépolymériser les mélanges de fibres de TEP et de fibres complexes à des températures modérées est prometteuse significative pour les opérations de recyclage industrielles pratiques, en particulier dans la gestion des déchets textiles mélangés difficiles à processus.
Les efforts de recherche futurs ciblent une optimisation plus approfondie de l'efficacité enzymatique à des températures de réaction encore plus faibles et dans les matériaux mélangés, facilitant finalement une adoption industrielle plus large et minimisant l'empreinte environnementale des efforts mondiaux de recyclage du plastique.