Une étude de l’École de médecine Icahn a découvert que l’asénapine, un médicament antipsychotique, peut agir via le récepteur TAAR1, révélant des différences cruciales entre le TAAR1 humain et celui des rongeurs. Cette découverte suggère de nouvelles voies pour traiter la consommation de substances et les troubles neuropsychiatriques et repenser les stratégies de développement de médicaments. Crédit : Issues.fr.com
L’étude met en lumière TAAR1, en soulignant les opportunités potentielles d’amélioration dans le développement de médicaments.
Des chercheurs de l’École de médecine Icahn du Mont Sinaï ont découvert des informations sur le mécanisme d’action potentiel de l’asénapine, un médicament antipsychotique, une cible thérapeutique possible pour la consommation de substances et les troubles neuropsychiatriques. Cette découverte pourrait ouvrir la voie au développement de médicaments améliorés ciblant la même voie.
Leurs conclusions, détaillées dans le numéro en ligne du 2 janvier de Communications naturellesmontrent qu’une protéine cérébrale connue sous le nom de récepteur TAAR1, une cible médicamenteuse connue pour réguler la signalisation de la dopamine dans les principales voies de récompense du cerveau, diffère considérablement chez l’homme par rapport aux modèles précliniques de rongeurs sur lesquels les médicaments sont généralement testés.
L’étude suggère de considérer espèces– des différences spécifiques dans les interactions médicament-récepteur et des recherches plus approfondies sur la manière dont l’asénapine affecte le corps, en tant qu’étapes vers des améliorations thérapeutiques potentielles.
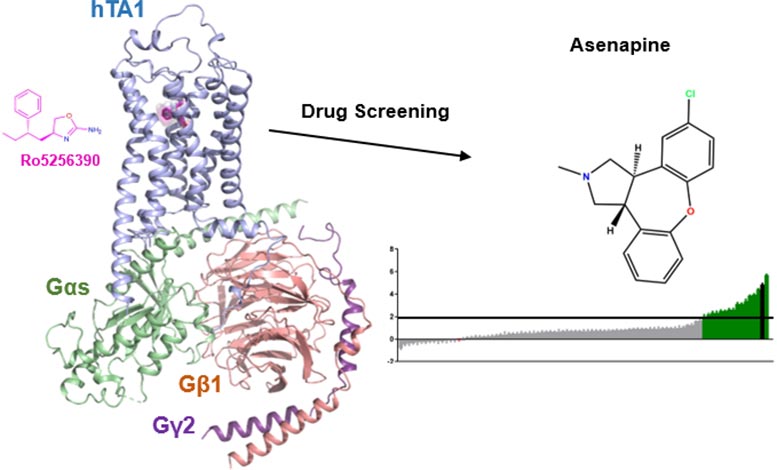
Les scientifiques du mont Sinaï Icahn ont pris des photos détaillées de la façon dont les médicaments peuvent se lier au récepteur TAAR1 à l’aide de CryoEM. Ils ont également découvert qu’un médicament antipsychotique, l’asénapine, active de manière inattendue TAAR1, ce qui pourrait potentiellement contribuer aux effets thérapeutiques de l’asénapine. Crédit : Wacker et al., Nature Communications
« En étudiant les propriétés fonctionnelles et structurelles de TAAR1, notre étude visait à faire la lumière sur ses mécanismes et sa pharmacologie », explique le premier auteur de l’étude, Gregory Zilberg, doctorant à Icahn Mount Sinai. « Nos résultats pourraient guider le développement de nouveaux médicaments TAAR1 et inciter à davantage d’exploration de médicaments similaires à l’asénapine. »
En utilisant des techniques avancées pour étudier la structure et la fonction de TAAR1, les chercheurs ont identifié trois éléments importants. Premièrement, il existe des différences entre les TAAR1 des rongeurs et des humains qui affectent probablement la manière dont les études sur modèles précliniques peuvent être transposées aux humains. Deuxièmement, TAAR1 est beaucoup plus étroitement lié aux récepteurs de la sérotonine et de la dopamine qu’on ne le pensait auparavant. Cela suggère que plusieurs médicaments ciblant la sérotonine pourraient avoir une efficacité thérapeutique inconnue ou des effets secondaires qui sont en fait dus à leurs actions sur TAAR1.
Enfin, les enquêteurs soulignent que l’asénapine, un antipsychotique utilisé en clinique, montre de manière inattendue une forte activation de TAAR1, ce qui suggère en fait que cet antipsychotique ciblant la sérotonine et la dopamine pourrait tirer certains de ses effets thérapeutiques de l’activation de TAAR1. Si cela est prouvé dans d’autres études, cela pourrait ouvrir de nouvelles possibilités pour son potentiel dans d’autres applications thérapeutiques liées à TAAR1, telles que son utilisation dans les troubles liés à l’usage de substances, ainsi que le développement de nouveaux médicaments à base d’asénapine.
Les chercheurs ont noté l’absence d’informations sur les différences dans le fonctionnement de TAAR1 chez les rongeurs et les humains, et ont souligné que certaines de ces différences pourraient expliquer pourquoi les données précliniques sur TAAR1 n’ont pas encore été traduites avec succès en thérapies efficaces chez l’homme. Ensuite, les chercheurs prévoient d’étudier où se trouve TAAR1 dans les cellules et quel est son rôle précis dans l’influence de la signalisation de la sérotonine et de la dopamine.
« Cette étude constitue une avancée significative dans la compréhension de TAAR1, offrant des pistes potentielles pour le développement de médicaments et encourageant la poursuite des recherches sur ses applications thérapeutiques », déclare l’auteur principal Daniel Wacker, PhD, professeur adjoint de sciences pharmacologiques., et neurosciences, à Icahn Mont Sinaï. « À mesure que nos travaux avancent, nous prévoyons qu’ils pourraient jouer un rôle crucial dans le développement de nouveaux médicaments ciblant TAAR1 et offrir des informations précieuses sur la façon dont des médicaments similaires à l’asénapine pourraient agir. »
Les autres auteurs co-auteurs de ce travail, tous avec Icahn Mount Sinai, sont Alexandra K. Parpounas, MS, Audrey L. Warren (candidat au doctorat) et Shifan Yang, PhD.




