L'ammoniac est utilisé dans les engrais et de nombreux processus industriels. Il est également considéré comme un moyen prometteur de stocker et de transporter l'énergie, car il est plus sûr et plus facile de gérer l'ammoniac que l'hydrogène gazeux. En utilisant le plasma, le quatrième état de matière, les scientifiques ont créé un matériau qui stimule la production d'ammoniac.
« Si l'on a besoin d'hydrogène industriel ailleurs que là où il est fabriqué, il sera plus facile et plus sûr de transporter l'hydrogène en tant qu'ammoniac et de le stocker jusqu'à ce qu'il soit nécessaire. Idéalement, alors on décomposerait l'ammoniac où l'hydrogène est nécessaire, à la demande », a déclaré Emily Carter, conseiller stratégique principal et directeur de laboratoire associé pour le service de laboratoire de matériaux et de durabilité de la durabilité des États-Unis. (PPPL).
« Ainsi, il faut des méthodes pour synthétiser et décomposer l'ammoniac de et à l'hydrogène efficacement et à moindre coût, et nous travaillons à la fois sur PPPL dans la division scientifique de l'électromation d'AMSS. »
La recherche a été effectuée par une équipe multidisciplinaire de diverses institutions, notamment le DOE's PPPL et Oak Ridge National Laboratory, Princeton University, Rutgers University et Rowan University. Un article sur l'œuvre a récemment été publié dans Lettres d'énergie ACS.
« La méthode actuelle de fabrication de l'ammoniac coûte cher », a déclaré Zhiyuan Zhang, candidat au doctorat à l'Université Rutgers-Newark et auteur principal de la recherche. « Vous avez besoin d'une grande usine pour faire de l'ammoniac en utilisant des processus qui nécessitent des températures et des pressions extrêmes. »
Stockage et transport de l'hydrogène sous forme d'ammoniac
L'ammoniac peut être utilisé comme support pour l'hydrogène, ce qui signifie qu'il peut stocker et transporter le produit chimique avant d'être converti en hydrogène pour l'énergie. L'hydrogène nécessite de grandes usines de fabrication et des installations de stockage. Cette nouvelle méthode pourrait créer de l'ammoniac dans des installations beaucoup plus petites situées plus près de l'endroit où elle est nécessaire, même potentiellement sur place. Si l'ammoniac doit être transporté de longues distances, cela serait également moins cher.
« L'hydrogène a une densité d'énergie très faible, et le déplacement de l'hydrogène est extrêmement difficile. L'ammoniac a une densité d'énergie plus élevée – deux fois par rapport à l'hydrogène comprimé – et peut être transporté sur de longues distances plus facilement que l'hydrogène », a déclaré Yiguang JU, un chercheur principal, un professeur de recherche principale de recherche. « Cela pourrait ouvrir un changement transformateur dans le stockage et le transport d'énergie. »
Mark Martirez, le conseiller adjoint de la science de la durabilité à l'AMSS et un physicien de la recherche, crée désormais des simulations de certaines des expériences détaillées dans le nouvel article afin que l'équipe puisse bien comprendre ce qui se passe lors de la réaction chimique au niveau atomique.
« Les simulations sont essentielles pour comprendre pleinement le mécanisme que les espèces chimiques subissent pour produire de l'ammoniac à partir de l'eau et de l'azote », a déclaré Marrez. « Ils ne pouvaient que deviner les positions des différents atomes basés sur une image de l'expérience. » Martirez apporte une compréhension rare de la chimie quantique impliquée dans le processus, qui est largement connu sous le nom de catalyse du plasma et est un domaine relativement nouveau.
Au lieu d'utiliser la chaleur élevée et la pression requises pour la catalyse thermique – l'ancienne approche pour faire de l'ammoniac à partir d'hydrogène et d'azote – la nouvelle méthode utilise l'électricité, l'eau, l'azote et le plasma à basse température. Dans le plasma à basse température, les molécules non chargées sont relativement froides ou à température ambiante. Cependant, les électrons sont très chauds. Les électrons ont suffisamment d'énergie pour changer la surface des catalyseurs, éliminant certains atomes et implantation d'azote ou d'atomes d'hydrogène dans leurs couches les plus à l'extérieur.
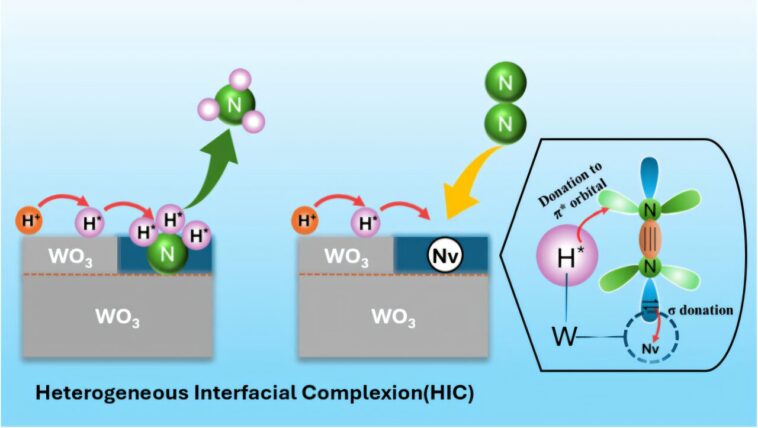
Un catalyseur est un ingrédient qui accélère les réactions chimiques sans changer dans le processus. Le catalyseur utilisé dans les expériences a une structure unique qui permet des transformations chimiques plus économes en énergie. Les scientifiques appellent cette structure un teint interfacial hétérogène (HIC).
« Les catalyseurs, l'oxyde de tungstène et l'oxynitride de tungstène, ne sont pas nouveaux. Ce qui est nouveau, c'est la structure et la méthode compatible plasma pour la fabriquer de manière contrôlable et évolutive », a déclaré Huixin He, professeur de l'Université Rutgers qui était l'un des principaux chercheurs de la recherche.
La structure du catalyseur est la clé de son efficacité
La conception spéciale du HIC aide à créer des atomes d'hydrogène hautement actifs là où ils sont nécessaires pour former de minuscules vides, appelés vacances en azote, qui sont un ajustement parfait pour une molécule d'azote. Ces caractéristiques fonctionnent ensemble: les atomes d'hydrogène convertissent l'azote en ammoniac, et les taches vacantes attirent plus d'azote de l'air pour maintenir le processus. Cette méthode augmente considérablement la quantité d'ammoniac produite par rapport aux méthodes plus anciennes. Il minimise également les réactions secondaires indésirables, comme la création d'hydrogène gazeuse au lieu de l'ammoniac.
« Le processus de production de ce catalyseur a été réduit d'environ deux jours à 15 minutes », a déclaré Zhang. Le processus a également surclassé d'autres méthodes similaires en termes de quantité d'ammoniac générée. Les chercheurs continueront d'étudier des moyens d'améliorer la production d'ammoniac avec le catalyseur HIC.
Sophia Kurdziel de PPPL; Christopher Kondratowicz, Yijie Xu, Elizabeth Desmet et Eddie Tang de l'Université de Princeton; Jacob Smith et Miaofang Chi du Oak Ridge National Laboratory; Pavel Kucheryavy, Junjie Ouyang et Michael Adeleke de l'Université Rutgers; et Aditya Dilip Lele de l'Université Rowan.