Dans un effort de collaboration, les chercheurs de l'Université d'Amsterdam et de l'Institut HFML-Felix de Nijmegen ont pu fournir des informations détaillées dans la structure moléculaire d'un organocatalyseur basé sur Thiourée, ainsi que les changements structurels précis subis lorsqu'ils sont liés à la liaison avec des réactifs. Ils ont élucidé la géométrie précise du catalyseur et du complexe de réact de catalyseur en utilisant le rayonnement infrarouge du laser électronique libre de Felix, combiné avec des expériences de faisceau moléculaire et des calculs chimiques quantiques.
Les chercheurs ont publié leurs résultats dans un article dans le Journal of Physical Chemistry Letters. Il ouvre la voie à la capture d'intermédiaires réactifs des réactions catalysées à la volée et donc à la conception rationnelle de nouveaux organocatalyseurs plus efficaces.
Permettre un contrôle précis
Les catalyseurs sont des composants cruciaux en chimie, permettant des conversions chimiques dans des processus aussi divers que la production alimentaire, la synthèse pharmaceutique et l'énergie durable. De nombreux catalyseurs sont à base de métaux, ce qui peut les rendre coûteux, respectueux de l'environnement et souvent toxiques.
Ces dernières années ont vu l'émergence d'organocatalyseurs, de petites molécules sans métal qui ont le potentiel d'être bon marché, stable, sûre et respectueuse de l'environnement. Ceux-ci peuvent également fournir une énantiosélectivité élevée, permettant un contrôle précis sur la formation de variantes conformationnelles préférées (énantiomères) de la même molécule – ce qui est de la plus haute importance en matière d'activité biologique.
Dans leur article récent, l'équipe de recherche d'Amsterdam-Nijmegen dirigée par le professeur Wybren Jan Buma de la photonique moléculaire présente une approche réussie pour déterminer la géométrie moléculaire précise des organocatalyseurs – dans leur état natif ainsi que pendant l'activité catalytique, lors de la liaison d'un réactif.
Ils ont étudié le mode d'action du «catalyseur de Takemoto» comme exemple d'une classe d'organocatalyseurs qui fonctionnent de manière enzymatique, en s'appuyant sur plusieurs liaisons hydrogène pour lier les réactifs dans une conformation fixe. L'obtention d'informations précises et fiables sur la structure du catalyseur et les interactions inter et intramoléculaires pertinentes est cruciale pour la conception rationnelle de nouveaux organocatalyseurs plus efficaces.

Des résultats plus difficiles et meilleurs
La méthode présentée par BUMA et ses collègues s'appuie sur la spectroscopie infrarouge à l'aide du laser Felix Free-Electron de l'Institut HFML-Felix, exploité par le NWO Dutch Research Council.
L'obtention d'empreintes digitales infrarouges d'intermédiaires impliquées dans les réactions catalytiques a été possible auparavant, mais uniquement pour les espèces ioniques qui sont beaucoup plus faciles à manipuler et à manipuler. Des études sur les réactions impliquant des espèces neutres sont restées à la portée.
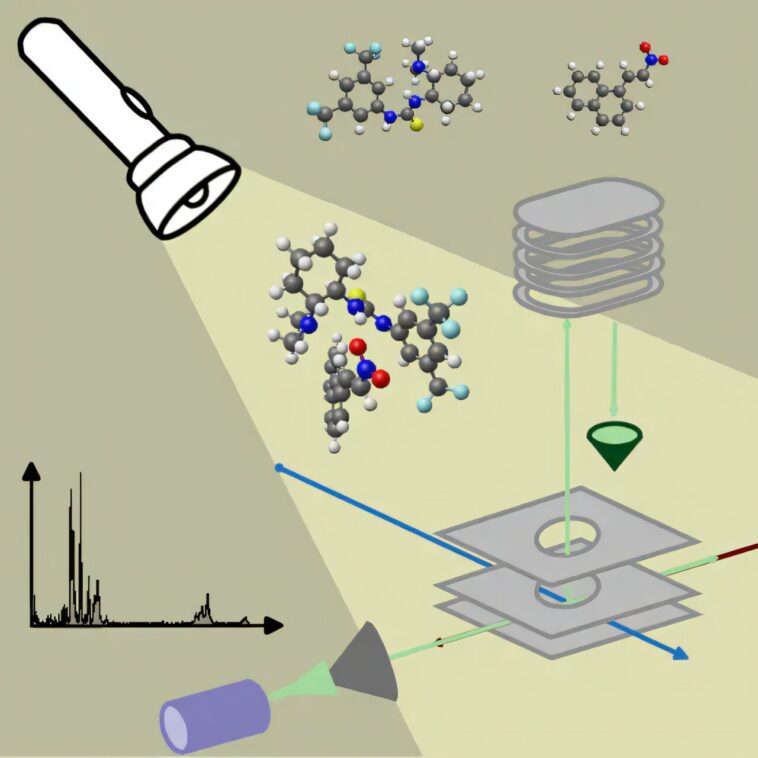
Les expériences ont été réalisées en fusionnant un faisceau moléculaire de catalyseur et de réactif avec la lumière laser infrarouge de Felix, qui donne accès à une large gamme spectrale (de 650 à 3500 cm-1). Les principales caractéristiques vibratoires des empreintes digitales du catalyseur lui-même se trouvent dans cette gamme, ainsi que des modes vibrationnels qui sont sensibles aux interactions subtiles avec le réactif de nitrooléfine.
Les chercheurs ont combiné les empreintes digitales IR détaillées (de structure, d'interactions intra et intermoléculaires et de formation de liaisons hydrogène) avec des calculs chimiques quantiques pour arriver à une caractérisation sans équivoque du catalyseur et du complexe de catalyseur-réactant, dans des détails sans précédent.
«Geler» l'intermédiaire réactif
Il est important de réaliser que dans le complexe de réact de catalyseur, le catalyseur doit adopter une structure complètement différente de celle du catalyseur isolé a une énergie beaucoup plus élevée. Les conditions de taux de collision élevées pendant l'expansion du faisceau moléculaire, cependant, nous permettent de « geler » l'intermédiaire réactif qui précède finalement le résultat final de la réaction. En tant que tel, la recherche a permis d'élucider le mode d'action du catalyseur.
Les présents résultats sont très prometteurs car ils apportent d'autres capacités à portée de main – par exemple, des études similaires sur les intermédiaires réactifs des réactions catalytiques impliquant plus d'un seul réactif. En outre, la méthodologie présentée est largement applicable, innovant ainsi de nouveaux terrains pour des études similaires sur un large éventail d'autres réactions catalo-catalysées par les organes et les métallos pertinents dont les intermédiaires réactifs sont restés jusqu'à présent insaisissables.