Lorsque les molécules d'ARN sont synthétisées par les cellules – un processus critique dans la création de protéines et d'autres fonctions cellulaires – elles subissent généralement une série d'événements « pliants » qui déterminent leur structure et le rôle qu'ils joueront dans l'expression d'informations génétiques dans les organismes vivants.
Jusqu'à récemment, cependant, on ne sait pas grand-chose sur ces processus de pliage qui se produisent très tôt dans la vie des molécules d'ARN.
Mais les chercheurs de Yale ont maintenant développé une méthode pour cartographier et mesurer la structure de l'ARN à mesure qu'elle se développe, une avance qui peut aider les scientifiques à concevoir des traitements plus efficaces pour une multitude de maladies. Leurs résultats sont décrits dans le journal Cellule moléculaire.
La structure d'un ARN détermine comment fonctionne la molécule, y compris si elle agit comme un ARNt (ARN de transfert), un ARNr (ARN ribosomal) ou un ARNm (ARN messager). Chacun de ces types de molécules joue des rôles cruciaux impliquant l'expression des informations génétiques, comme déterminer la quantité de protéines faites à partir d'un ARNm. Dans certains cas, ont constaté que les scientifiques ont constaté que les mutations qui affectent le repliement contribuent directement aux maladies génétiques.
(Le processus est appelé repliement parce que la nature chimique de l'ARN – composé de quatre nucléotides a, c, g et u – répète les nucléotides individuels dans une partie de la molécule pour interagir avec d'autres nucléotides dans la même molécule.)
« Notre nouvelle méthode nous permet de visualiser les premières structures que les ARN forment. Jusqu'à présent, nous ne connaissions que les structures matures », a déclaré Leonard Schärfen, un doctorat. candidat au département de biophysique et de biochimie moléculaire de Yale et auteur principal de l'étude. « Les premières structures pourraient avoir des fonctions distinctes qui pourraient être ciblées par des thérapies qui ne fonctionnent pas sur les ARN matures. »
Karla Neugebauer, auteur principal de l'étude et professeur de biophysique et de biochimie moléculaire de R Selden Rose à la Faculté des arts et des sciences de Yale et de la Yale School of Medicine, a qualifié l'œuvre de « tour de force technique de LEO » avec le potentiel de réglementer l'expression des gènes très tôt dans la vie d'un ARN. Neugebauer est également professeur de biologie cellulaire et directeur du Yale Center for ARN Science and Medicine.

La méthode développée par les chercheurs, qu'ils appellent le suivi de la structure co-transcriptionnelle (CostSeq), est capable de détecter la première activité de pliage de l'ARN dans les cellules vivantes.
La méthode, disent-ils, combine deux principes biochimiques distincts.
« Premièrement, nous isolons très spécifiquement les molécules d'ARN à un moment de leur synthèse », a déclaré Schärfen, qui fait partie de la Graduate School of Arts and Sciences de Yale. « Ensuite, nous ajoutons un produit chimique qui modifie l'ARN et nous permet d'étudier la structure à mesure que les molécules se développent plus longtemps avec le temps. »
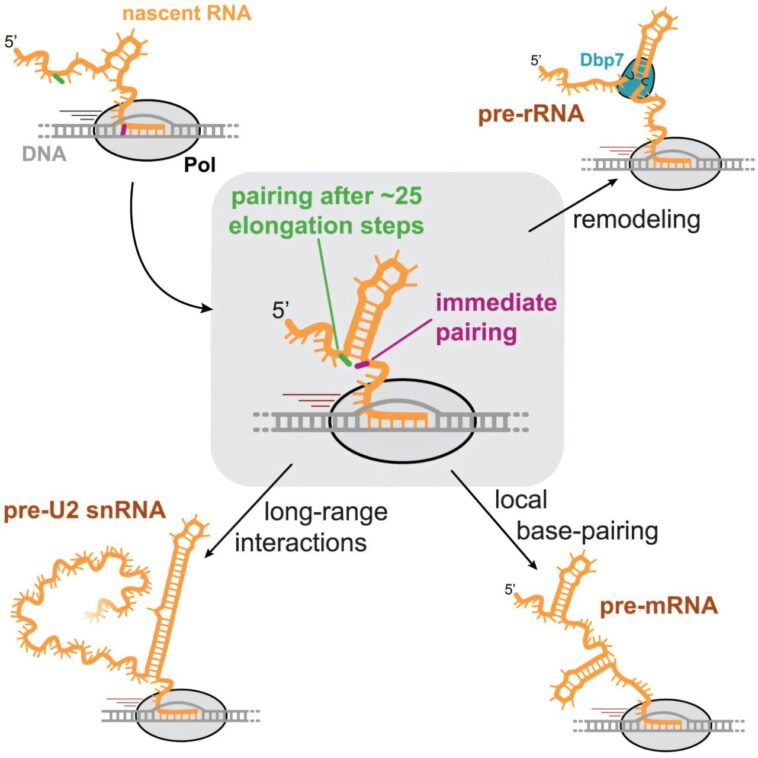
Parmi leurs résultats, les chercheurs ont découvert que les molécules d'ARN commencent à se replier immédiatement dès qu'ils émergent de l'ARN polymérase, le complexe protéique qui les synthétise. Cette découverte souligne l'importance du pliage précoce pour l'expression saine des gènes et peut apporter un nouvel éclairage sur les maladies causées par l'ARN mal replié, disent-ils.
Ils ont également constaté que dans l'ARNm, le pliage précoce dicte la forme pliée finale, de sorte que la structure moléculaire est définie dès le début. Dans l'ARNr, cependant, les premières formes sont temporaires et réorganisent avant la définition d'une molécule. Une protéine appelée DBP7, une enzyme d'hélicase, joue un rôle crucial dans le processus de remodelage de l'ARNr, aidant une molécule à se replier dans sa structure finale.
D'autres auteurs de l'étude sont Matthew D. Simon, professeur agrégé de biophysique moléculaire et de biochimie et membre de l'Institut de conception et de découverte biomoléculaires, et Isaac Vock, chercheur étudiant diplômé en biophysique moléculaire et biochimie.