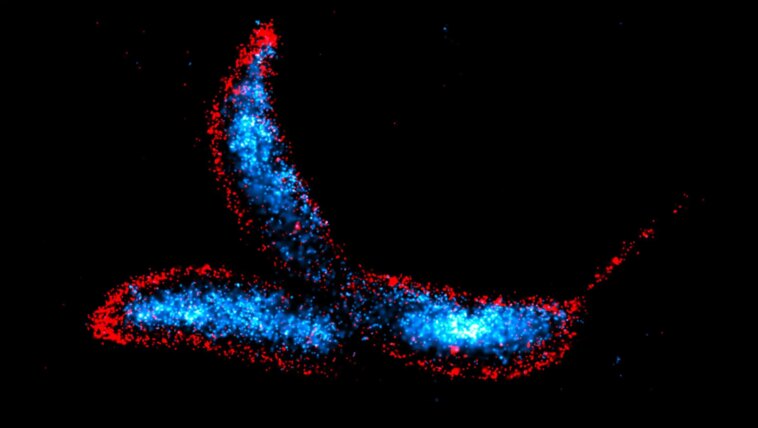
Caulobacter croissant est une bactérie dimorphe en forme de croissant qui sert de l’un des principaux organismes modèles pour étudier la régulation du cycle cellulaire bactérien, la différenciation cellulaire et la morphogenèse. Les cellules ont été visualisées en utilisant la technique DNA-PAINT, avec l’ADN chromosomique coloré en bleu et les membranes cellulaires colorées en rouge. Crédit : Institut Max Planck de microbiologie terrestre/Hernandez-Tamayo
Comment une protéine régulatrice agit comme un multi-outil de remodelage de la paroi cellulaire bactérienne.
Pour que les cellules bactériennes se développent et se divisent, leurs parois cellulaires doivent être continuellement remodelées. Ce processus nécessite un équilibre minutieux entre les enzymes lytiques et la production de peptidoglycanes. Une équipe de chercheurs dirigée par Martin Thanbichler a découvert qu’un régulateur central peut contrôler des classes complètement différentes d’autolysines. Étant donné que de nombreux antibiotiques attaquent la paroi cellulaire bactérienne, cette découverte pourrait ouvrir la voie à de nouvelles méthodes de traitement contre les infections bactériennes.
Au cours de l’évolution, les cellules ont développé un large éventail de stratégies pour renforcer leur enveloppe contre la pression osmotique interne, leur permettant ainsi de se développer dans une variété d’environnements différents. Le plus bactérien espèces synthétiser une paroi cellulaire semi-rigide entourant la membrane cytoplasmique, dont le composant principal, le peptidoglycane, forme un maillage dense qui enveloppe la cellule.
En plus de son rôle protecteur, la paroi cellulaire sert également de moyen pour générer des formes cellulaires spécifiques, telles que des sphères, des bâtonnets ou des spirales, facilitant ainsi la motilité, la colonisation de surface et la pathogénicité.
La présence d’une paroi cellulaire présente ses propres défis : les cellules doivent constamment la remodeler pour croître et se diviser. Pour ce faire, ils doivent très soigneusement faire des déchirures dans le mur pour lui permettre de s’étendre et de changer, tout en comblant rapidement les lacunes avec du nouveau matériau pour l’empêcher de s’effondrer. Ce processus de remodelage de la paroi cellulaire implique le clivage des liaisons par des enzymes lytiques, également appelées autolysines, et l’insertion ultérieure d’un nouveau matériau de paroi cellulaire par des peptidoglycanes synthases. Les activités de ces deux groupes de protéines antagonistes doivent être étroitement coordonnées pour éviter les points faibles de la couche de peptidoglycane qui conduisent à la lyse et à la mort des cellules.
L’équipe de recherche dirigée par Martin Thanbichler, Max Planck Fellow à l’Institut Max Planck de microbiologie terrestre et professeur de microbiologie à l’Université de Marburg, a entrepris de démêler la composition et la fonction de la machinerie autolytique. Leurs études portent sur la bactérie en forme de croissant Caulobacter croissantqui se trouve dans les environnements d’eau douce et largement utilisé comme organisme modèle pour étudier les processus cellulaires fondamentaux chez les bactéries.
Selon Thanbichler, étudier la fonction des autolysines a été une tâche difficile. « Bien que nous en sachions beaucoup sur les machines synthétiques, les autolysines se sont avérées être un problème difficile à résoudre. » Maria Billini, chercheuse postdoctorale dans l’équipe de Thanbichler, ajoute : « Les bactéries abritent généralement de nombreux types d’autolysines de différentes familles d’enzymes avec des cibles différentes. Cela signifie que ces protéines sont hautement redondantes et que la suppression de gènes d’autolysine individuels a souvent peu d’effet sur la morphologie et la croissance des cellules.
Détendeur polyvalent
L’analyse des régulateurs potentiels de l’autolysine par criblage par co-immunoprécipitation et tests d’interaction protéine-protéine in vitro a révélé qu’un facteur appelé DipM joue un rôle central dans le remodelage de la paroi cellulaire bactérienne. Ce régulateur clé, une protéine périplasmique soluble, interagit de manière surprenante avec plusieurs classes d’autolysines ainsi qu’avec un facteur de division cellulaire, montrant une promiscuité jusqu’alors inconnue pour ce type de régulateur.
DipM a été capable de stimuler l’activité de deux enzymes de clivage du peptidoglycane avec des activités et un repliement complètement différents, ce qui en fait le premier régulateur identifié capable de contrôler deux classes d’autolysines. Notamment, les résultats indiquent également que DipM utilise une interface unique pour interagir avec ses différentes cibles.
« La perturbation de DipM entraîne la perte de régulation à divers points du processus de remodelage et de division de la paroi cellulaire et tue finalement la cellule », déclare le doctorant Adrian Izquierdo Martinez, premier auteur de l’étude. « Sa fonction appropriée en tant que coordinateur de l’activité de l’autolysine est donc essentielle pour le bon maintien de la forme cellulaire et la division cellulaire dans C. croissant.”
La caractérisation complète de DipM a révélé un nouveau réseau d’interaction, y compris une boucle auto-renforcée qui relie les transglycosylases lytiques et éventuellement d’autres autolysines au cœur de l’appareil de division cellulaire de C. croissant, et très probablement aussi d’autres bactéries. Ainsi, DipM coordonne un réseau complexe d’autolysines dont la topologie diffère grandement de celle des systèmes d’autolysines précédemment étudiés. Martin Thanbichler souligne : « L’étude de ces régulateurs multi-enzymes, dont le dysfonctionnement affecte plusieurs processus liés à la paroi cellulaire en même temps, ne nous aide pas seulement à comprendre comment la paroi cellulaire réagit aux changements de la cellule ou de l’environnement. Il peut également contribuer au développement de nouvelles stratégies thérapeutiques qui combattent les bactéries en perturbant simultanément plusieurs voies autolytiques.