La vie est devenue plus difficile pour ceux qui luttent contre les superbactéries résistantes aux antibiotiques. Des chercheurs de l'Université McGill ont découvert deux enzymes qui utilisent un mécanisme inédit pour conférer une résistance, ouvrant ainsi un tout nouveau front dans la lutte contre la résistance aux antimicrobiens (RAM), l'un des 10 principaux problèmes de santé publique mondiaux.
Albert Berghuis, professeur à l'Université McGill, et Mark Hemmings, titulaire d'un doctorat. étudiant dans son laboratoire, étudiaient les types d'enzymes qui provoquent la résistance aux antibiotiques lorsqu'ils ont vu une structure que personne n'avait jamais vue auparavant. De nombreuses enzymes de résistance agissent en imitant la cible de l'antibiotique à l'intérieur de la cellule bactérienne, en interceptant et en désactivant le médicament avant qu'il ne puisse faire son travail.
Mais ils ont découvert deux enzymes qui attaquent les antibiotiques aminoglycosides sans utiliser cette approche de mimétisme cible. Les aminosides sont une classe d'antibiotiques à large spectre utilisés pour traiter les infections bactériennes graves.
« Nous avons trouvé deux enzymes qui n'imitent pas du tout la cible », explique Berghuis. « Alors, nous nous sommes demandé : est-ce toujours des superbactéries ? »
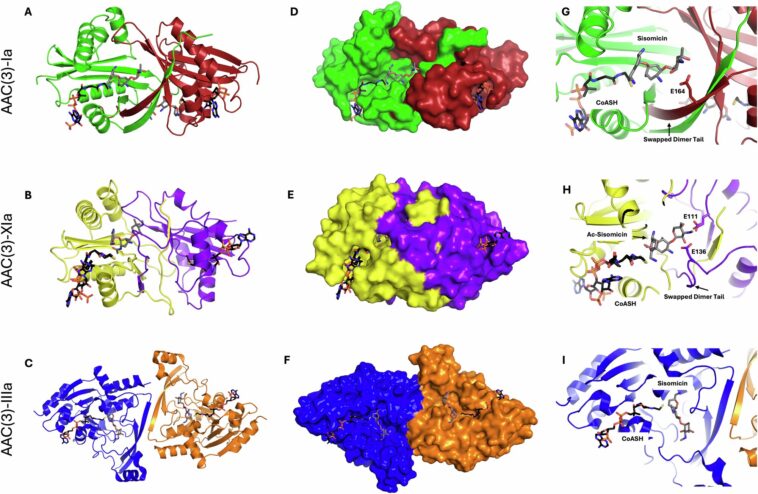
Les chercheurs ont utilisé la Canadian Light Source de l'Université de la Saskatchewan pour examiner la structure moléculaire des enzymes et des médicaments auxquels elles se lient. Ils ont constaté que les enzymes, appelées AAC(3)-Ia et AAC(3)-XIa, se lient au médicament lorsque sa structure annulaire centrale est tordue en forme de bretzel plutôt qu'en son disque plat habituel.
Cela ne semblait pas être un mécanisme de résistance particulièrement efficace. Les molécules d'aminosides ne passent qu'environ 0,1 % de leur temps sous forme de bretzel, explique Berghuis, ce qui ne laisse pas beaucoup de possibilités aux enzymes de les saisir et de les désactiver.
« Nous ne nous attendions pas à ce qu'ils soient de très bonnes enzymes », explique Hemmings, mais les résultats ont été une surprise : AAC(3)-XIa a largement dépassé leurs attentes. « L'un d'eux était plutôt mauvais, mais l'autre est en réalité tout aussi bon que ceux qui ciblent le mimétisme. » Les chercheurs affirment que des recherches supplémentaires sont nécessaires pour déterminer comment l'enzyme peut être efficace lorsqu'elle est si rarement en mode « attaque ». Les découvertes de l'équipe sont publiées dans la revue Chimie des communications.
Berghuis affirme que ces travaux devraient contribuer à la lutte contre la résistance aux antibiotiques, en soulignant le fait qu'il existe plus de types d'enzymes susceptibles de provoquer une résistance que nous ne le pensions. Les chercheurs devront prendre plus au sérieux ces enzymes non conventionnelles lorsqu’elles seront identifiées dans le génome des bactéries.
« Avant, nous aurions ignoré ce genre d'enzymes, mais maintenant nous devons en tenir compte », dit-il. « Le problème (de la résistance aux antibiotiques) s'est développé et a rendu la vie plus compliquée. »