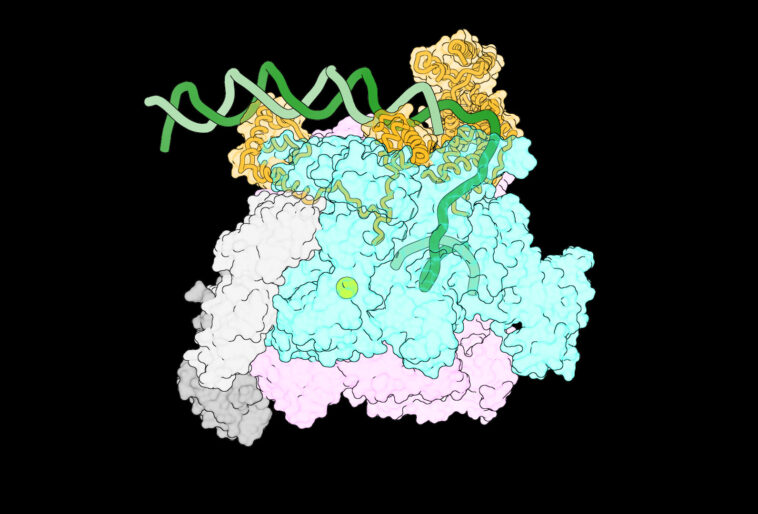
L'une des premières images des complexes intermédiaires qui se forment lorsque l'ARN polymérase rencontre l'ADN. Crédit : Laboratoire de biophysique moléculaire de l'université Rockefeller
Des découvertes récentes illustrent comment ARN la polymérase interagit avec ADN pour initier la transcription, capturée en quelques millisecondes à l'aide de techniques de microscopie avancées. Cette avancée apporte de nouvelles perspectives sur les mécanismes régulant l'expression des gènes, contribuant ainsi à résoudre des débats de longue date dans ce domaine.
Chaque cellule vivante transcrit l'ADN en ARN. Ce processus démarre lorsqu'une enzyme appelée ARN polymérase (ARNP) se fixe à l'ADN. En quelques centaines de millisecondes, la double hélice d'ADN se déroule, formant une bulle de transcription, permettant à un brin d'ADN exposé d'être copié en un brin d'ARN complémentaire.
On ne sait pas vraiment comment la RNAP parvient à cet exploit. Un instantané de la RNAP en train d'ouvrir cette bulle fournirait une mine d'informations, mais le processus se déroule trop rapidement pour que la technologie actuelle puisse facilement capturer des visualisations de ces structures. Aujourd'hui, une nouvelle étude Nature Biologie structurale et moléculaire décrit l'ARN polymérase d'E. coli en train d'ouvrir la bulle de transcription.
Les résultats, obtenus en 500 millisecondes de mélange de l'ARN polymérase et de l'ADN, éclairent les mécanismes fondamentaux de la transcription et répondent à des questions de longue date sur le mécanisme d'initiation et l'importance de ses différentes étapes. « C'est la première fois que quelqu'un parvient à capturer des complexes de transcription transitoires au moment où ils se forment en temps réel », explique la première auteure, Ruth Saecker, spécialiste de recherche au laboratoire de Seth Darst à Rockefeller. « Comprendre ce processus est crucial, car il s'agit d'une étape régulatrice majeure de l'expression génétique. »
Une vue inédite
Darst a été le premier à décrire la structure de l'ARN polymérase bactérienne, et l'étude de ses subtilités est restée l'un des principaux objectifs de son laboratoire. Alors que des décennies de travail ont établi que la liaison de l'ARN polymérase à une séquence spécifique d'ADN déclenche une série d'étapes qui ouvrent la bulle, la manière dont l'ARN polymérase sépare les brins et positionne un brin dans son site actif reste un sujet de débat passionné.
Les premiers travaux dans ce domaine suggéraient que l’ouverture des bulles ralentissait considérablement le processus, dictant la vitesse à laquelle l’ARN polymérase peut passer à la synthèse de l’ARN. Des résultats ultérieurs dans ce domaine ont remis en question cette idée, et de nombreuses théories ont émergé sur la nature de cette étape limitant la vitesse. « Nous savions, grâce à d’autres techniques biologiques, que, lorsque l’ARN polymérase rencontre l’ADN pour la première fois, elle crée un ensemble de complexes intermédiaires hautement régulés », explique le coauteur Andreas Mueller, chercheur postdoctoral au laboratoire. « Mais cette partie du processus peut se dérouler en moins d’une seconde, et nous n’avons pas pu capturer des structures sur une échelle de temps aussi courte. »
Pour mieux comprendre ces complexes intermédiaires, l’équipe a collaboré avec des collègues du Centre de biologie structurale de New York, qui ont développé un système robotisé à jet d’encre capable de préparer rapidement des échantillons biologiques pour une analyse par cryomicroscopie électronique. Grâce à ce partenariat, l’équipe a capturé des complexes se formant dans les 100 à 500 premières millisecondes de la rencontre de l’ARN polymérase et de l’ADN, ce qui a permis d’obtenir des images de quatre complexes intermédiaires distincts suffisamment détaillées pour permettre l’analyse.
Pour la première fois, une image claire des changements structurels et des intermédiaires qui se forment au cours des étapes initiales de la liaison de l'ARN polymérase à l'ADN est apparue. « La technologie a été extrêmement importante pour cette expérience », explique Saecker. « Sans la capacité de mélanger rapidement l'ADN et l'ARN polymérase et d'en capturer une image en temps réel, ces résultats n'existent pas. »
Se mettre en position
En examinant ces images, l'équipe a pu décrire une séquence d'événements montrant comment l'ARN polymérase interagit avec les brins d'ADN lors de leur séparation, avec un niveau de détail jusqu'alors inédit. Au fur et à mesure que l'ADN se déroule, l'ARN polymérase s'accroche progressivement à l'un des brins d'ADN pour empêcher la double hélice de se reconstituer. Chaque nouvelle interaction provoque un changement de forme de l'ARN polymérase, ce qui permet la formation de nouvelles connexions protéine-ADN. Cela comprend l'expulsion d'une partie d'une protéine qui empêche l'ADN de pénétrer dans le site actif de l'ARN polymérase. Une bulle de transcription stable se forme ainsi.
L'équipe suggère que l'étape limitant la vitesse de transcription pourrait être le positionnement du brin d'ADN matrice dans le site actif de l'enzyme RNAP. Cette étape implique de surmonter d'importantes barrières énergétiques et de réorganiser plusieurs composants. Les recherches futures viseront à confirmer cette nouvelle hypothèse et à explorer d'autres étapes de la transcription.
« Nous n’avons étudié que les toutes premières étapes de cette étude », explique Mueller. « Nous espérons ensuite examiner d’autres complexes, des étapes ultérieures et d’autres étapes du cycle de transcription. »
Au-delà de la résolution des théories contradictoires sur la manière dont les brins d’ADN sont capturés, ces résultats soulignent l’intérêt de la nouvelle méthode, qui permet de capturer des événements moléculaires se produisant en quelques millisecondes en temps réel. Cette technologie permettra de nombreuses autres études de ce type, aidant les scientifiques à visualiser les interactions dynamiques dans les systèmes biologiques.
« Si nous voulons comprendre l’un des processus les plus fondamentaux de la vie, que toutes les cellules effectuent, nous devons comprendre comment sa progression et sa vitesse sont régulées », explique Darst. « Une fois que nous saurons cela, nous aurons une idée beaucoup plus claire de la manière dont la transcription commence. »