Une étude menée par des chercheurs de CUNY ASRC, utilisant la cristallographie aux rayons X dans différentes conditions, a révélé diverses formes d’une protéine liée à une maladie, offrant ainsi de nouvelles voies pour le développement de médicaments. Crédit : Issues.fr.com
De nouvelles expériences de cristallographie utilisant une pression et une chaleur élevées pour révéler comment les protéines changent de forme pourraient faire progresser le développement de nouveaux médicaments.
Les protéines font le gros du travail en remplissant les fonctions biochimiques de notre corps en se liant à des métabolites ou à d’autres protéines pour accomplir des tâches. Pour y parvenir, les molécules de protéines changent souvent de forme pour permettre des interactions de liaison spécifiques nécessaires à l’exécution de processus chimiques complexes et précis.
Recherche sur les structures des protéines
Une meilleure compréhension des formes que prennent les protéines donnerait aux chercheurs des informations importantes sur la manière de stopper ou de traiter les maladies, mais les méthodes actuelles permettant de révéler ces formes dynamiques et tridimensionnelles offrent aux scientifiques des informations limitées.
Pour combler ce manque de connaissances, une équipe du Advanced Science Research Center du CUNY Graduate Center (CUNY ASRC) a conçu une expérience pour tester si la réalisation d’une imagerie par cristallographie aux rayons X utilisant une température élevée par rapport à une pression élevée révélerait des formes distinctes. Les résultats des travaux de l’équipe seront publiés aujourd’hui (12 janvier) dans la revue Biologie des communications.
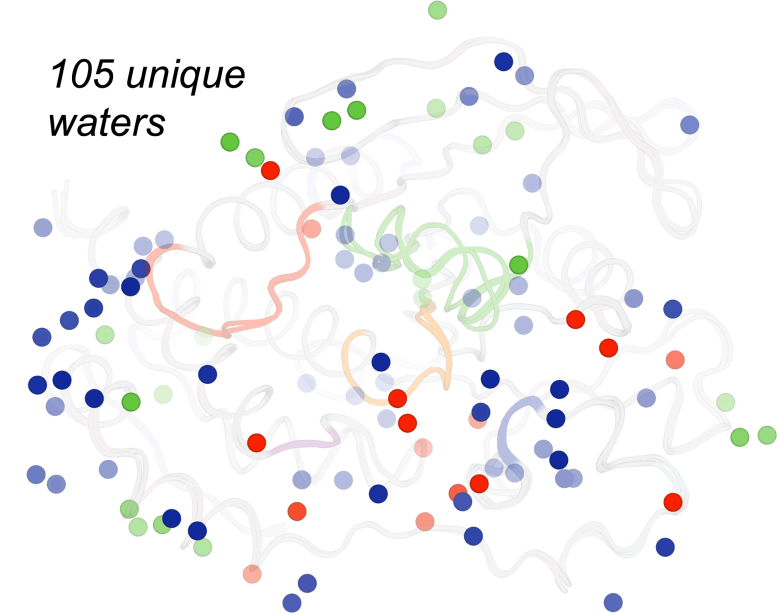
Les positions de ces molécules d’eau sont souvent importantes pour comprendre la flexibilité des protéines et la capacité des molécules médicamenteuses à influencer la structure et la fonction des protéines. Dans cette étude, différentes eaux uniques sont apparues à la surface de la protéine sous différentes perturbations expérimentales telles qu’une température élevée (rouge), une haute pression (vert) ou des conditions par défaut (bleu), offrant des informations complémentaires sur ces questions. Crédits : Ali Ebrahim et Liliana Guerrero
Aperçus de l’étude par le Dr Daniel Keedy
« Les structures protéiques ne restent pas immobiles ; ils se déplacent entre plusieurs formes similaires, un peu comme un danseur », a déclaré le chercheur principal de l’étude, Daniel Keedy, Ph.D., professeur à l’Initiative de biologie structurale de la CUNY ASRC et professeur de chimie et de biochimie au City College de New York et à la CUNY. Centre d’études supérieures. « Malheureusement, les approches existantes pour visualiser les protéines ne révèlent qu’une seule forme ou suggèrent la présence de plusieurs formes sans fournir de détails spécifiques. Nous voulions voir si différentes manières d’examiner une protéine pouvaient nous donner une vue plus détaillée de la façon dont elle change de forme.
Expérimentation et observations
Pour leur expérience, l’équipe a obtenu des cristaux de STEP, également connu sous le nom de PTPN5, une protéine cible d’un médicament pour le traitement de plusieurs maladies, notamment Alzheimer– et les a agités en utilisant soit une haute pression (2 000 fois la pression atmosphérique de la Terre), soit une haute température (température corporelle), toutes deux très différentes des expériences de cristallographie typiques à pression atmosphérique et à température cryogénique (-280 °F,-173 °C). Les chercheurs ont examiné les échantillons par cristallographie aux rayons X et ont observé que la température et la pression élevées avaient des effets différents sur la protéine, révélant des formes distinctes.
Implications pour le développement de médicaments
Bien que la haute pression ne soit pas une condition que subissent les protéines à l’intérieur du corps, Keedy a déclaré que la méthode d’agitation a exposé différents états structurels de la protéine qui peuvent être pertinents pour son activité dans les cellules humaines.
« Avoir la capacité d’utiliser des perturbations telles que la chaleur et la pression pour élucider ces différents états pourrait donner aux développeurs de médicaments des outils pour déterminer comment ils peuvent piéger une protéine dans une forme particulière en utilisant un médicament à petite molécule pour diminuer sa fonction », a ajouté Keedy.




