Champignon à capuchon doré (Psilocybe cubensis). Crédit : Felix Blei/Leibniz-HKI, édité
Une nouvelle étude met en lumière la structure et l’évolution d’une enzyme chez les champignons psychoactifs.
La substance psychoactive psilocybine est le produit naturel le plus important des « champignons magiques » du genre Psilocybe, ce qui fait de ces champignons une drogue populaire. Cependant, la psilocybine est également devenue de plus en plus intéressante en médecine ces dernières années pour un certain nombre de maladies mentales. Il a montré des résultats prometteurs dans le traitement de la dépression, de la dépendance et de l’anxiété. La psilocybine se trouve donc déjà à un stade avancé d’essais cliniques en tant qu’ingrédient pharmaceutique actif.
La psilocybine est formée par des champignons lors de processus biochimiques complexes à partir des acides aminés acide L-tryptophane. L'enzyme PsiM, une méthyltransférase, joue un rôle important dans ce processus. Il catalyse successivement deux réactions de méthylation, les deux dernières étapes de la production de psilocybine.
«Il existe de nombreuses réactions de transfert de méthyle dans la nature», explique Dirk Hoffmeister. Il est professeur de microbiologie pharmaceutique à l'Université Friedrich Schiller de Jena et dirige un groupe de recherche associé à l'Institut Leibniz pour la recherche sur les produits naturels et la biologie des infections – Institut Hans Knöll (Leibniz-HKI). « Ici, nous nous sommes demandé comment s'effectuait exactement la production de psilocybine. »
Deux enzymes, une origine
À cette fin, une équipe de l’Université de médecine d’Innsbruck dirigée par le cristallographe Bernhard Rupp et les chercheurs de Jena ont étudié l’enzyme PsiM à la fois biochimiquement et par analyse de la structure cristalline aux rayons X. Cette méthode permet de visualiser les protéines jusqu’au niveau atomique, ce qui permet de représenter plusieurs étapes de la réaction en ultra-haute résolution.
L'examen de la structure protéique a révélé d'étonnantes similitudes de structure entre l'enzyme fongique PsiM et les enzymes qui sont normalement responsables de la modification de ARN. Bien qu’il existe également des différences, la grande similitude structurelle indique que l’enzyme fongique a évolué à partir d’une seule ARN méthyltransférase méthylante. En conséquence, il n’avait auparavant la capacité d’attacher qu’un seul groupe méthyle à la molécule cible.
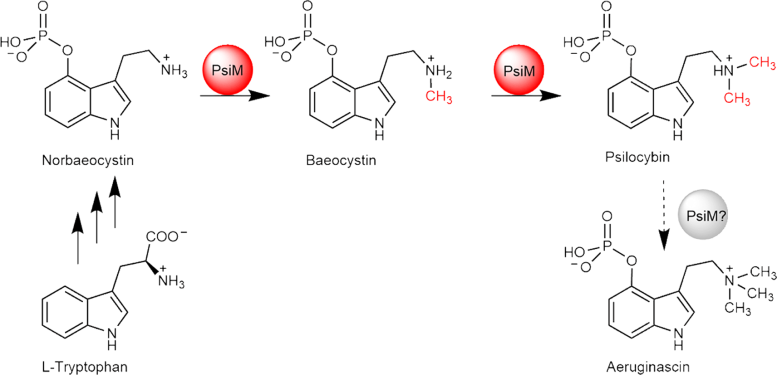
La biosynthèse de la psilocybine commence avec le L-tryptophane et implique deux étapes de méthylation catalysées par le PsiM. Crédit : Dirk Hoffmeister/Leibniz-HKI
« Le précurseur de la psilocybine, la norbaéocystine, qui est converti par le PsiM, imite structurellement une partie de l'ARN, mais est méthylé deux fois », explique Hoffmeister.
Un petit échange avec un grand impact
Dans des recherches plus approfondies, les chercheurs ont également pu identifier un échange crucial d'acides aminés qui a donné à PsiM la capacité d'effectuer une double méthylation au cours de l'évolution. Ce processus implique la dernière étape de toute la chaîne de réaction pour une production biotechnologique potentielle du principe actif : la conversion de la baéocystine intermédiaire simple méthylée en psilocybine double méthylée.
Une fin claire
Les chercheurs se sont alors demandé si le PsiM pouvait également convertir la psilocybine en aéruginascine en y attachant un troisième groupe méthyle. L'aéruginascine est un analogue de la psilocybine, présente naturellement dans certains types de champignons. « La seule question est : d’où vient-il ? demande Hoffmeister.
Jusqu'à présent, il y avait un désaccord au sein de la communauté scientifique quant à savoir si le composé est un produit métabolique de la voie de biosynthèse de la psilocybine et pourrait provenir de la psilocybine via le PsiM. L’étude fournit désormais un résultat clair : « Ce n’est clairement pas le cas », déclare Hoffmeister. « PsiM n'est pas capable de convertir la psilocybine en aéruginascine. » Le PsiM peut donc être exclu pour la production biosynthétique de cet analogue.
Cependant, l’enzyme pourrait à l’avenir être pertinente pour la production de psilocybine dans des micro-organismes : « Dans l’ensemble, nos résultats peuvent aider à développer de nouvelles variantes de psilocybine dotées de propriétés thérapeutiques améliorées et à les produire de manière biotechnologique », explique Hoffmeister.




