Des chercheurs de l'Université nationale de Singapour (NUS) ont conçu une méthode pour « s'éteindre » en toute sécurité et temporairement « , puis » activer « l'acide ribonucléique (ARN) à l'intérieur des cellules. Ceci est réalisé en utilisant des groupes chimiques contenant du disulfure optimisé structurellement qui s'attachent à l'ARN et le maintiennent inactif jusqu'à ce que les conditions à l'intérieur de la cellule éliminent naturellement ces groupes, rétablissant la fonction d'ARN normale. Cette stratégie pourrait potentiellement ouvrir de nouvelles avenues dans des thérapies et une modification génétique basés sur l'ARN plus précis.
Les résultats sont publiés dans la revue Édition internationale d'Angewandte Chemie.
L'ARN a acquis une importance en tant que plate-forme thérapeutique de nouvelle génération. Cependant, il est toujours difficile de livrer l'ARN en toute sécurité au bon endroit dans le corps et de l'activer uniquement lorsque et où il est nécessaire. Les méthodes de livraison d'ARN existantes, comme les nanoparticules lipidiques, les limitations du visage, y compris les effets secondaires possibles, l'efficacité limitée et le manque de contrôle précis.
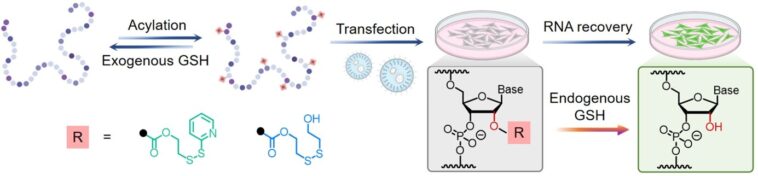
Pour résoudre ces problèmes, une équipe de recherche dirigée par le professeur adjoint Zhu Ru-yi du Département de chimie de NUS a développé une approche post-synthétique purement chimique qui « cages » ARN temporairement en modifiant ses sites 2'-OH avec des groupes acyle contenant un disulfure soigneusement réglé.
Ces modifications peuvent temporairement empêcher l'ARN de mener à bien son activité biologique naturelle jusqu'à ce que le glutathion intracellulaire (GSH), un agent réducteur commun, agit comme la « clé » en déclenchant une réaction redox qui élimine les groupes acyle.
En ajustant la structure chimique et les propriétés de ces groupes acyle, les chercheurs peuvent obtenir une activation d'ARN rapide, efficace et contrôlable pour divers types d'ARN, des brins synthétiques courts aux ARN messager longs (ARNm).
Le professeur adjoint Zhu a déclaré: « Notre approche fournit une méthode universelle pour moduler l'activité de l'ARN avec un contrôle spatial et temporel, sans s'appuyer sur des enzymes ou de la lumière. Il s'agit du premier exemple d'une activation de l'ARNm réactive qui a été démontrée à la fois dans les environnements de tube à essai et de cellules vivants. »
Grâce à une série d'optimisations systématiques, l'équipe a établi trois méthodes chimiques distinctes pour acyler l'ARN post-synthétiquement. Ces méthodes permettent le blocage réversible de la fonction de l'ARN et peuvent être déclenchées pour libérer l'ARN par des GSH naturels ou à fournit à l'extérieur.
L'ARN modifié a démontré une excellente stabilité, une activation sélective et une récupération fonctionnelle réussie in vitro et dans les cellules vivantes. Notamment, lorsqu'il est appliqué à l'édition du gène CRISPR-CAS9 et à la traduction de l'ARNm, les ARN sensibles aux redox ont pu regagner pleinement leur activité lors du traitement GSH, mettant en évidence la polyvalence du système.
Surtout, cette stratégie ne reposait pas sur des systèmes de livraison volumineux ou des déclencheurs externes potentiellement nocifs, ce qui le rend attrayant à de futures applications en biologie synthétique, en thérapeutique à l'ARN et en livraison intracellulaire.
« La simplicité et une large compatibilité de notre système d'acylation sensible à l'oxydat redox le rendent accessible à un large éventail de chercheurs travaillant avec l'ARN », a ajouté le professeur adjoint Zhu.
Pour l'avenir, l'équipe conçoit de nouveaux outils chimiques et des modifications réactives de l'ARN pour affiner davantage le contrôle de l'activité de l'ARN dans les systèmes vivants. Leur objectif est de permettre des thérapies basées sur l'ARN plus précises et programmables pour les futures applications médicales et de recherche.