La recherche sur le φX174, un bactériophage, révèle son potentiel dans le traitement des infections résistantes aux antibiotiques. Historiquement important en phagothérapie et en biologie moléculaire, le mécanisme unique de lyse cellulaire du φX174 pourrait ouvrir la voie à des antibiotiques innovants.
φX174, un bactériophage étudié pour son potentiel dans la lutte contre les bactéries résistantes aux antibiotiques, offre de nouvelles perspectives dans le développement d’antibiotiques alternatifs.
À l’âge de COVID 19le mot « virus» suscite des pensées de contagion, de maladie et même de mort. Mais que se passerait-il s’il existait un virus – un tout petit virus capable de se répliquer des centaines de fois toutes les demi-heures – qui pourrait guérir une infection bactérienne grave résistante à tous les antibiotiques connus ? C’est cet espoir qui motive Bil Clemons, professeur de biochimie Arthur et Marian Hanisch Memorial, à rechercher le virus nommé φX174.
Comprendre φX174
φX174 est un bactériophage ou, plus simplement, un phage : un virus qui cible les cellules bactériennes. D’un point de vue humain, φX174 mène une vie simple : il trouve sa bactérie hôte, se gare à sa surface, injecte un brin de ADN dans la cellule bactérienne, réplique son ADN encore et encore, force la cellule à fabriquer des protéines virales, assemble l’ADN et les protéines en de nouveaux virions (copies du phage), puis brise la paroi cellulaire de la bactérie afin que les virions puissent trouver d’autres hôtes à infecter.
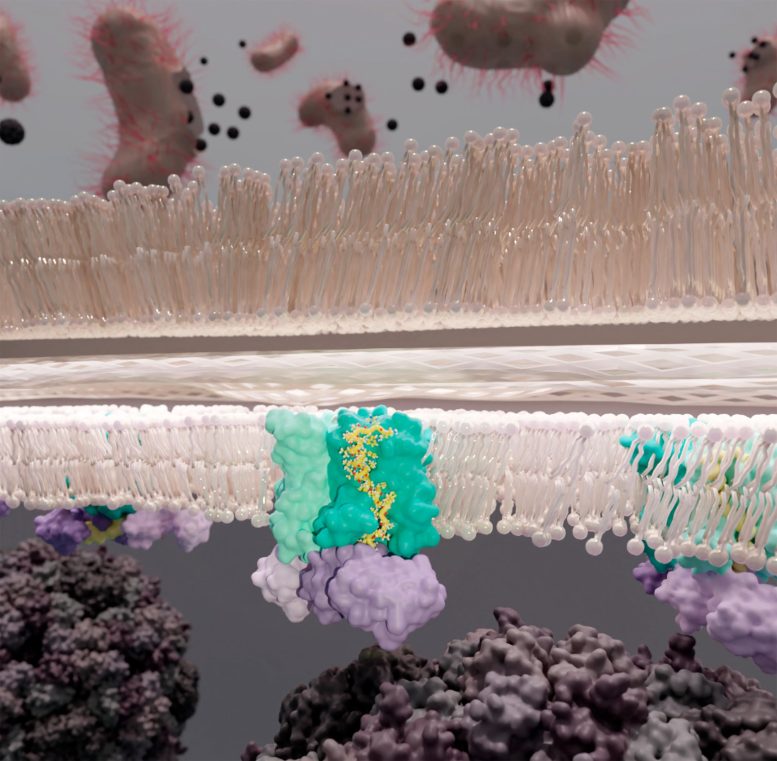
L’évasion de ΦX174 de son hôte bactérien. Dans la membrane se trouve le complexe OUI (enzyme MraY d’E. coli (cyan), protéine de phage E (jaune) et chaperon d’E. coli SlyD (violet)) où la protéine E perturbe la synthèse du peptidoglycane en inhibant MraY, permettant ainsi la rupture de la paroi cellulaire ( bronzer). Crédit : Karen Orta
C’est ce mécanisme d’évasion que l’équipe Clemons élucide dans son article récemment publié dans la revue
Science
, « Le mécanisme de l’antibiotique protéique codé par le phage à partir de φX174. » En s’appuyant sur des images de cryomicroscopie électronique à particule unique, il est révélé que la protéine E de φX174 se joint aux protéines MraY et SlyD de son hôte bactérien pour former un complexe stable, le complexe OUI. Il en résulte une lyse cellulaire : la brèche de la paroi cellulaire bactérienne et la mort de la bactérie.
Contexte historique de la découverte des phages
φX174 est sur le radar des scientifiques depuis environ 100 ans. Au début du XXe siècle, l’existence des phages n’était que théorisée. Travaillant indépendamment, le bactériologiste britannique Frederick Twort et le scientifique québécois Félix d’Herelle ont postulé l’existence de phages en se basant sur le comportement des cultures bactériennes dans leurs laboratoires. Parfois, lorsque les bactéries étaient censées proliférer sur leurs boîtes de Pétri, des taches brillantes (des plaques) apparaissaient là où aucune bactérie ne se développait. Le passage de ces échantillons à travers des filtres a capturé les bactéries tout en permettant à leurs minuscules tueurs invisibles de passer. Quoi que ce soit qui ait réussi à passer à travers les filtres, il était trop petit pour être vu au microscope.
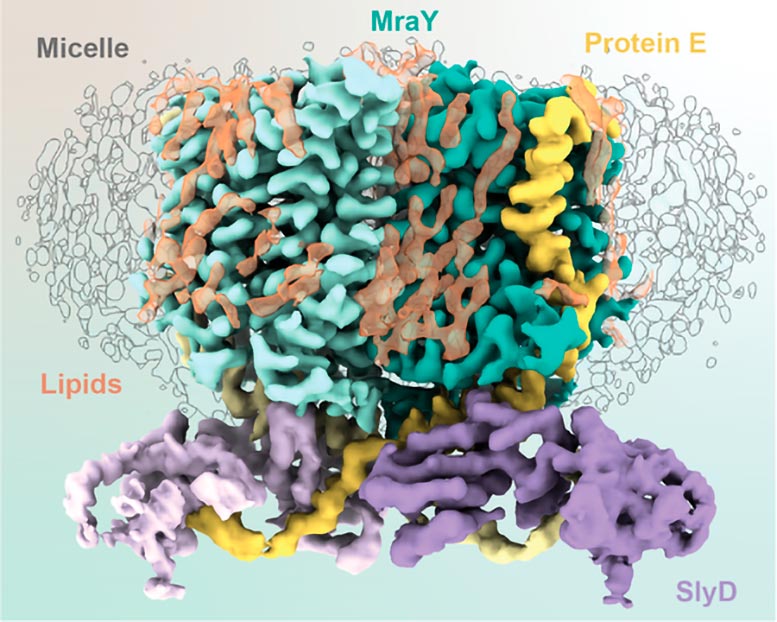
Schéma des éléments composant le complexe OUI. Crédit : Karen Orta
D’Herelle, travaillant à Paris en 1917, suggéra que ces tueurs devaient être des virus mangeurs de bactéries et était prêt à tester cette théorie. Selon la légende urbaine, comme le raconte Clemons, d’Hérelle filtrait les eaux usées à plusieurs reprises, puis les buvait pour voir si elles pouvaient être consommées sans danger. Il se sentit indemne, alors il offrit une gorgée à son assistant de laboratoire, qui était également inchangé. D’Hérelle a ensuite donné les eaux usées filtrées à un patient, un jeune garçon atteint de dysenterie sévère et sur le point de mourir. Grâce à ce cocktail de phages, qui comprenait très probablement du φX174, le garçon a rapidement recouvré la santé.
Des chercheurs de toute l’Europe sont venus à Paris pour travailler avec d’Herelle. L’un de ces chercheurs, le microbiologiste croate Vladimir Sertič, a passé une décennie à travailler dans le laboratoire de d’Herelle. C’est Sertič et son assistant, Nikolai Boulgakov, qui ont conçu une taxonomie des phages connus. Le nom à consonance exotique de φX174, dans le système de classification de Sertic, signifie simplement « le 174ème virus de la dixième (chiffre romain X) série de phages qui ciblent plusieurs bactéries », de la classe φ : les phages qui agissent contre plusieurs bactéries. La thérapie phagique continue de guérir les maladies bactériennes, mais elle tue aussi, probablement parce que les chercheurs ne savaient pas encore comment purifier les sous-produits de la réplication des phages, tels que les débris bactériens, qui peuvent être toxiques.
Évolution de la phagothérapie et de la recherche
La recherche et la thérapie sur les phages se sont fragmentées sous la pression de la Seconde Guerre mondiale. Pour les alliés occidentaux, la production de pénicilline très efficace a complètement éclipsé la phagothérapie, devenant ainsi la solution unique aux infections bactériennes. La pénicilline était un secret militaire qui n’était pas partagé avec les alliés de l’Est ou les puissances de l’Axe, c’est pourquoi les médecins soviétiques ont continué à utiliser les phages à des fins thérapeutiques, une pratique qui persiste aujourd’hui dans les pays de l’ex-Union soviétique.
Bien que les phages soient tombés en disgrâce auprès des chercheurs en médecine des pays occidentaux dans les décennies qui ont suivi la Seconde Guerre mondiale, les chercheurs scientifiques sont devenus fascinés par eux. φX174, bien que n’étant qu’un parmi des milliards de types de phages différents, est passé au premier plan en tant qu’outil expérimental utile pour le domaine en développement de la biologie moléculaire.
Robert L. Sinsheimer, professeur de biophysique à Caltech de 1957 à 1977, a joué un rôle déterminant dans le développement du φX174 comme organisme modèle. Son laboratoire a réalisé la cartographie du génome de φX174 et a découvert bon nombre de ses caractéristiques les plus intrigantes. Alors que Sinsheimer racontait l’histoire dans une interview d’histoire orale en 1991, il invita Max Delbrück, professeur de biologie à Caltech, à donner une série de conférences à l’Université d’État de l’Iowa au début des années 1950, où Sinsheimer faisait alors partie du corps professoral. « Il (Delbrück) nous a époustouflés avec son travail sur les phages », a déclaré Sinsheimer. « C’était absolument glorieux. »

Max Delbrück avec un groupe de phages, 1949. De gauche à droite : Jean Jacques Weigle, Ole Maaloe, Elie Wollman, Gunther S. Stent, Max Delbrück et G. Soli. Crédit : Ross Madden, Black Star. 1949-02, 1.3.1-16, photographies Caltech. Archives et collections spéciales de l’Institut de technologie de Californie
Delbrück, qui avait initialement suivi une formation de physicien à l’Université de Göttingen avant la guerre, constituait un groupe de chercheurs sur les phages au Caltech et utilisait les virus pour sonder les mystères de la génétique moléculaire. Sinsheimer s’est donné pour mission de venir à Caltech pendant un congé de six mois en 1953 pour apprendre à travailler avec les phages. Un jour, alors qu’ils discutaient dans le bureau de Delbrück de la manière de procéder en virologie, les deux hommes ont conclu qu’il pourrait être bénéfique d’étudier les phages les plus petits et potentiellement les plus simples pour mieux comprendre la structure et la réplication virales. Sinsheimer a examiné les phages candidats, a opté pour φX174, a acquis des échantillons auprès de laboratoires d’Angleterre et de France et s’est mis au travail.
C’est ainsi qu’a commencé une série de premières scientifiques basées sur φX174. Dans un essai de 1966, Sinsheimer a qualifié φX174 de « multum in parvo » : le latin signifiant « beaucoup en peu ». Tout au long des années 1950 et 1960, le φX174 n’a cessé de surprendre les chercheurs. En 1959, deux ans après avoir rejoint Caltech, Sinsheimer a déterminé que φX174 ne contenait qu’un seul brin d’ADN qu’il injectait dans la cellule hôte pour commencer la réplication. C’était une surprise étant donné que l’on avait découvert que l’ADN avait une structure à double hélice quelques années plus tôt. En 1962, Sinsheimer a émis l’hypothèse que l’ADN de φX174 avait la forme d’un anneau circulaire, ce que les biologistes moléculaires n’avaient pas encore visualisé. En 1977, Frederick Sanger de l’Université de Cambridge fut le premier à séquencer complètement un génome, ce qui lui valut le prix Nobel de chimie en 1980. Ce génome appartenait à φX174. Le phage lui-même a été acquis auprès de Sinsheimer.

Robert Sinsheimer dans son laboratoire, 1974. Crédit : Floyd Clark. 10.24-116, photographies Caltech. Archives et collections spéciales de l’Institut de technologie de Californie
À la fin des années 1970, une grande partie du cycle de vie du φX174 était bien comprise, mais des incertitudes subsistaient. On a supposé que le φX174 s’est libéré de son hôte bactérien en bloquant la synthèse de la couche de peptidoglycane – une barrière protectrice clé dans la paroi cellulaire de toutes les bactéries – tout comme le font la pénicilline et d’autres antibiotiques pharmaceutiques.
Pour la plupart des phages, les scientifiques avaient appris comment ils fabriquent des enzymes spécialisées, les endolysines, qui dégradent les acides aminés et les sucres. acide polymère qui constitue la couche de peptidoglycane. Mais ces enzymes sont trop volumineuses pour être contenues dans l’ADN d’un minuscule phage comme φX174.
Recherche moderne sur φX174
« Le génome du φX174 est vraiment petit », explique Clemons. « Si vous deviez coder quelque chose qui réalise la lyse cellulaire de la même manière qu’un lysozyme – une enzyme présente dans nos larmes et notre salive qui assure une protection contre les bactéries en imitant les endolysines – il n’y aurait pas de place pour d’autres protéines sur le génome φX174. φX174 fait partie d’un groupe de ces virus qui sont trop petits pour avoir une machinerie de lyse complexe, ces phages ont donc dû développer des moyens très simples de lyser les cellules bactériennes.
Différents phages et antibiotiques interfèrent avec la synthèse du peptidoglycane à différents moments du processus. La protéine E de φX174 cible MraY, une enzyme membranaire qui catalyse la synthèse d’un précurseur du peptidoglycane. Pour achever son travail destructeur, la protéine E de φX174 a besoin d’une autre protéine, SlyD, qu’elle détourne de son hôte bactérien. « C’est un mystère », dit Clemons, « parce que SlyD n’a aucune raison d’agir ici. Il n’interagit normalement pas avec MraY, il a un travail totalement différent. Pourtant, d’une manière ou d’une autre, ce processus nécessite SlyD.
Ces trois agents, un viral et deux provenant de l’hôte, constituent le complexe OUI : MraOuiprotéine E, SlyD. Essentiellement, la protéine E de φX174 s’entrelace avec MraY, inhibant l’activité enzymatique de MraY. SlyD lie et stabilise le complexe protéine E et MraY sans contacter MraY.
Implications pour le développement futur des antibiotiques
Cette découverte devrait aider les chercheurs à remplir la promesse initiale des bactériophages en tant qu’antibiotique thérapeutique. Les antibiotiques ont sauvé d’innombrables vies au cours du siècle dernier, mais l’invention de nouvelles classes d’antibiotiques n’a pas réussi à suivre la capacité des bactéries à développer une résistance à ces antibiotiques. Les bactéries mutent également pour résister aux phages, mais contrairement aux antibiotiques pharmaceutiques qui nécessitent un effort humain considérable pour améliorer leur structure, les phages eux-mêmes peuvent muter, contrecarrant ainsi les nouvelles défenses bactériennes. Nous vivons avec un nombre considérable de phages dans notre corps, plusieurs centaines de milliards. Clemons et d’autres chercheurs dans le domaine espèrent que rassembler les bons phages au bon moment pour lutter contre les infections bactériennes pourrait créer un nouvel antibiotique plus durable, dont nous avons de plus en plus besoin face aux bactéries résistantes aux antibiotiques.
Les co-auteurs de « Le mécanisme de l’antibiotique protéique codé par le phage de φX174 » incluent Anna K. Orta, Nadia Riera, Evelyn Yancheng Li, Shiho Tanaka, Hyun Gi Yun et Lada Klaic. Le financement a été assuré par le Instituts nationaux de la santé et la Fondation G. Harold et Leila Y. Mathers.