Des recherches récentes mettent en évidence le rôle unique du tissu adipeux omental dans l’inhibition de la formation de nouvelles cellules graisseuses, offrant ainsi de nouvelles approches potentielles pour les traitements et la gestion ciblés de l’obésité.
Comprendre la formation et la fonction des tissus adipeux est essentiel pour lutter contre l’obésité et les troubles métaboliques associés. Cependant, le comportement du tissu adipeux, communément appelé graisse corporelle, varie en fonction de sa localisation au sein du corps.
Prenez, par exemple, l'omentum : un gros tissu adipeux en forme de tablier suspendu à l'estomac et recouvrant les organes du péritoine, tels que l'estomac et les intestins. Il stocke non seulement les graisses, mais joue également un rôle dans la régulation immunitaire et la régénération des tissus.
Le tissu adipeux omental est associé à la forme du corps en « pomme », qui apparaît lorsque ce dépôt de graisse se développe de manière significative, augmentant ainsi le risque de maladies métaboliques. Cette expansion n’est pas due à la formation de nouvelles cellules adipeuses, un processus appelé adipogenèse, mais principalement à l’agrandissement des cellules existantes, un processus appelé hypertrophie. Cela peut entraîner une inflammation chronique et insuline résistance.
Recherche sur la graisse omentale
La capacité limitée de la graisse omentale à former de nouvelles cellules adipeuses, malgré un excès de calories, contraste avec la graisse sous-cutanée et reste mal comprise. Aujourd'hui, des scientifiques dirigés par le professeur Bart Deplancke de l'EPFL ont identifié une population de cellules dans le tissu adipeux omental humain qui entrave l'adipogenèse. La découverte, publiée dans Métabolisme cellulaireoffre un nouvel angle sur la capacité limitée de la graisse omentale à réaliser l'adipogenèse et a des implications significatives pour la gestion de l'obésité.
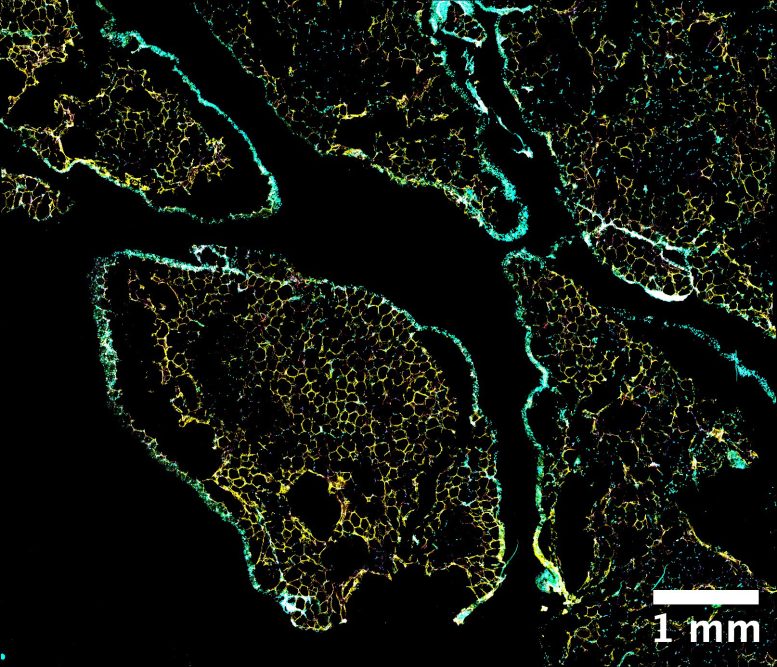
Images fluorescentes de microscopie confocale d'une coupe de tissu adipeux omental humain (graisse viscérale), représentant la couche de cellules mésothéliales entourant les lobules des adipocytes. Dans l'image, les adipocytes sont visualisés à l'aide d'une coloration contre la périlipine 1 (PLIN1, en jaune), tandis que les cellules mésothéliales sont colorées à l'aide de TM4SF1 (vert) et MSLN (rose). La coloration DAPI a été utilisée pour visualiser les noyaux cellulaires (cyan). Crédit : Radiana Ferrero et Julie Russeil (EPFL)
Les chercheurs ont utilisé des cellules unicellulaires avancées ARN séquençage pour analyser les cellules de divers dépôts de graisse humaine, isoler différentes sous-populations cellulaires et tester leur capacité à se transformer en nouvelles cellules adipeuses. L’étude, soutenue par plusieurs institutions médicales, dont le CHUV, a impliqué plus de trente donneurs humains pour effectuer une comparaison détaillée de différentes localisations graisseuses.
L’approche a identifié une population de cellules présentes dans le tissu adipeux omental qui pourrait bien être la clé pour expliquer ses propriétés inhabituelles. Ces cellules, appelées cellules mésothéliales, tapissent généralement certaines cavités internes du corps comme couche protectrice.
Transitions cellulaires et influence métabolique
Parmi ces cellules mésothéliales, certaines se sont étrangement rapprochées des cellules mésenchymateuses, qui peuvent se développer en divers types de cellules, notamment les adipocytes (cellules adipeuses). Cette transition dynamique entre les états cellulaires pourrait constituer un mécanisme clé par lequel ces cellules exercent leur influence sur le potentiel adipogénique du tissu adipeux omental.
L’étude a révélé que les propriétés de type mésenchymateux de ces cellules sont associées à une capacité accrue à moduler leur microenvironnement, fournissant ainsi un mécanisme de régulation permettant de limiter l’expansion du tissu adipeux. En alternant entre ces deux états, les cellules pourraient ainsi influencer le comportement métabolique global du dépôt graisseux omental et sa capacité à accumuler des graisses sans déclencher de complications métaboliques.
«Nous avons également découvert au moins une partie du mécanisme moléculaire par lequel cette nouvelle population de cellules omentales affecte l'adipogenèse», explique Radiana Ferrero (EPFL), l'une des principales auteurs de l'étude. « Plus précisément, les cellules expriment des niveaux élevés d’IGFBP2 (Insulin-like Growth Factor Binding Protein 2), une protéine connue pour inhiber l’adipogenèse, et sécrètent cette protéine dans le microenvironnement des cellules. Cela affecte à son tour des récepteurs spécifiques sur les cellules souches adipeuses et progénitrices voisines, les empêchant efficacement de se développer en cellules adipeuses matures.
«Ces résultats ont de profondes implications pour la compréhension et potentiellement la gestion de l'obésité métaboliquement malsaine», explique Pernille Rainer (EPFL), autre chercheuse principale de l'étude. « Savoir que la graisse omentale possède un mécanisme intégré pour limiter la formation de cellules adipeuses pourrait conduire à de nouveaux traitements modulant ce processus naturel. En outre, la recherche ouvre la voie à des thérapies ciblées susceptibles de moduler le comportement de dépôts graisseux spécifiques.
L'étude a été financée par l'École Polytechnique Fédérale de Lausanne, la Fondation Leenaards, la santé personnalisée et les technologies associées (PHRT) et le Fonds national suisse (FNS).




