Des chercheurs de la Tokyo Metropolitan University ont développé une nouvelle méthode de détermination de la structure en utilisant la spectroscopie de résonance magnétique nucléaire (RMN) qui montre comment différentes parties des machines moléculaires complexes comme les enzymes se déplacent pendant qu'ils aident à catalyser les réactions. La recherche est publiée dans le Journal de l'American Chemical Society.
En se concentrant sur une enzyme dans la levure, ils démontrent comment les contrastes des mouvements à l'échelle atomique ont un impact sur leur fonction. La méthode promet un accès sans précédent aux mécanismes par lesquels les biomolécules fonctionnent et comment elles se rapportent aux maladies.
Les enzymes sont indispensables à la fonction de tous les organismes biologiques, y compris les humains. Alors que les instantanés capturés à l'aide de la microscopie aux rayons X ou cryo-électrons ont révélé leur structure moléculaire complexe, ils sont un flou constant de mouvement lorsqu'ils sont à l'œuvre.

Leur structure à l'échelle atomique change constamment, capturant d'autres biomolécules et les aidant à réagir dans une séquence soigneusement chorégraphiée. Bien que clairement importants, ces mouvements rapides à l'échelle nanométrique sont difficiles à capturer.
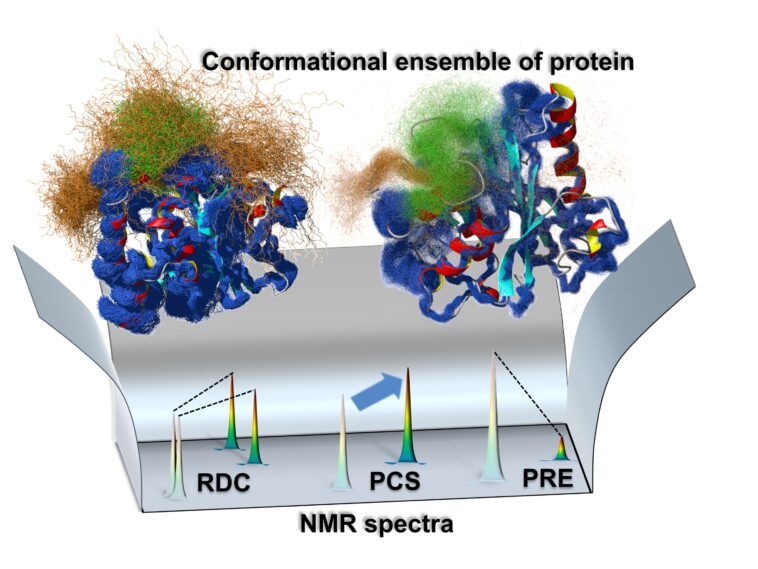
En intégrant une combinaison d'approches différentes, les chercheurs dirigés par le professeur agrégé Teppei Ikeya de l'Université métropolitaine de Tokyo « structure d'ensemble » d'une enzyme de réaction. Essentiellement, la structure d'ensemble est la collection de tous les états qu'une macromolécule peut prendre, et quelle est la probabilité de prendre chacun.
L'équipe a démontré sa méthode avec l'ubiquitine hydrolase 1 de levure (YUH1), une enzyme dans la levure qui l'aide à recycler l'ubiquitine, une protéine qui régule divers événements intracellulaires.
YUH1 a un analogue chez l'homme appelé ubiquitine c-terminal hydrolase (UCHL1), connu pour être impliqué dans les maladies de Parkinson et d'Alzheimer. En intégrant plusieurs méthodes analytiques en utilisant la spectroscopie RMN, ils ont pu créer une carte d'ensemble pour YUH1 pour la dynamique sur l'échelle de temps en millisecondes.

Ils ont découvert que deux parties de l'enzyme près de la partie active, où les protéines sont liées, ont montré des mouvements frappants, un « boucle croisée » Structure et l'extrémité N, une extrémité de la structure de capture des protéines de l'enzyme.
L'extrémité N-terminale se déplaçait dans et hors de la boucle, passant par toute une gamme d'états avant de capturer finalement une protéine cible comme un lasso avant d'agir comme un « couvercle de déclenchement, » le garder en place. Ce nouveau mécanisme a été soutenu par la manière dont les versions mutantes « couvercles de déclenchement » Échec de la même activité enzymatique.
Les résultats de l'équipe révèlent comment la nature dynamique des enzymes joue un rôle important dans leur fonctionnement.
La méthode peut être appliquée à un vaste éventail de structures biologiques dans leur environnement naturel, promettant une nouvelle approche pour que les scientifiques accédent aux mécanismes sous-jacents et aux pathologies potentielles.