Des chercheurs du Mont Sinaï ont découvert comment la protéine TIMP2 affecte l’hippocampe, une zone du cerveau vitale pour la mémoire et l’apprentissage. En utilisant des techniques avancées sur des modèles de souris mutantes, l’équipe a montré que la diminution des niveaux de TIMP2 entraînait une réduction de la plasticité et de la fonction de mémoire.
Les chercheurs ont révélé comment la protéine TIMP2 régule la plasticité cérébrale, en particulier dans l’hippocampe, offrant ainsi de nouvelles perspectives dans le traitement des troubles liés à l’âge comme Alzheimer en ciblant la matrice extracellulaire du cerveau.
Les scientifiques du Mont Sinaï ont apporté un éclairage précieux sur le mécanisme d’une protéine clé qui régule la plasticité et la fonction de l’hippocampe, une région cérébrale clé impliquée dans la mémoire et l’apprentissage, et qui diminue avec l’âge chez la souris.
Les conclusions de l’équipe, publiées dans Psychiatrie Moléculairepourrait ouvrir la voie à une meilleure compréhension de la façon dont la protéine, connue sous le nom d’inhibiteur tissulaire des métalloprotéinases 2 (TIMP2), pourrait potentiellement être ciblée dans les troubles liés à l’âge comme la maladie d’Alzheimer pour aider à restaurer les processus moléculaires affectés dans le cerveau.
Comprendre le vieillissement et les troubles neurodégénératifs
Le vieillissement est connu pour être le principal facteur de risque de nombreuses maladies neurodégénératives, dont la maladie d’Alzheimer. Des travaux antérieurs menés par des chercheurs du mont Sinaï et d’autres ont révélé que les protéines enrichies dans le sang jeune, notamment TIMP2, pourraient être exploitées pour rajeunir la fonction cérébrale chez les animaux âgés en affectant la plasticité (ou la flexibilité des processus neuronaux liés à la mémoire) dans l’hippocampe. Malgré cette découverte importante, on savait peu de choses sur la biologie de la manière dont TIMP2 régule la plasticité de l’hippocampe au niveau moléculaire.
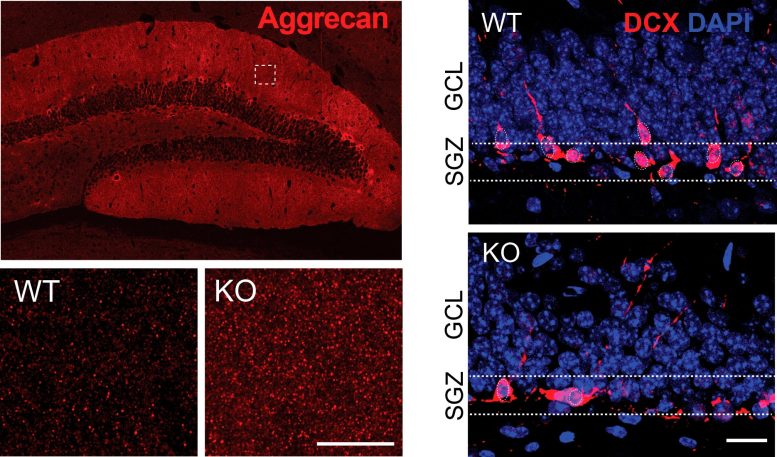
Accumulation de contenu de matrice extracellulaire dans le cerveau de souris « KO » déficientes en TIMP2 (colonne de gauche) qui conduit à des processus de plasticité altérés, y compris la migration des neurones nés adultes (colonne de droite). Crédit : Système de santé du Mont Sinaï
Aperçu du mécanisme moléculaire de TIMP2
« Dans notre dernière étude, nous avons détaillé un lien moléculaire impliquant cette protéine qui relie les processus de plasticité, y compris la génération de nouveaux neurones à l’âge adulte, à la nature structurelle – ou ce que nous appelons la matrice extracellulaire – du microenvironnement de l’hippocampe », explique Joseph. Castellano, PhD, professeur adjoint de neurosciences et de neurologie à l’École de médecine Icahn du Mont Sinaï et auteur principal de l’article. « TIMP2 contrôle ces processus en modifiant la flexibilité du microenvironnement grâce aux composants de la matrice extracellulaire. L’étude des voies qui régulent la matrice extracellulaire pourrait être importante pour concevoir de nouvelles thérapies pour les maladies dans lesquelles la plasticité est affectée.
Méthodes et résultats de recherche innovants
Pour leur travail, l’équipe a utilisé un modèle de souris mutante imitant la perte des niveaux de TIMP2 dans le sang et l’hippocampe, connue pour se produire avec l’âge. L’équipe a également créé un modèle qui a permis aux chercheurs de cibler et de supprimer spécifiquement le pool de TIMP2 exprimé par les neurones de l’hippocampe. Ces modèles, en combinaison avec ARN le séquençage, l’imagerie confocale, la microscopie à super-résolution et les études comportementales ont permis un examen moléculaire détaillé de la régulation de la plasticité de TIMP2.
Les chercheurs, dont la première auteure Ana Catarina Ferreira, PhD, boursière postdoctorale dans le groupe du Dr Castellano, ont appris que la perte de TIMP2 entraîne une accumulation de composants de la matrice extracellulaire dans l’hippocampe qui se produit parallèlement à une réduction des processus de plasticité, y compris la génération des neurones nés à l’âge adulte, de l’intégrité synaptique et de la mémoire. La matrice extracellulaire est un réseau de nombreux composants macromoléculaires qui constituent le microenvironnement structurel autour et entre les cellules.
Implications et orientations futures de la recherche
« Nous avons directement ciblé ce phénotype avec une enzyme délivrée à l’hippocampe qui affecte la matrice extracellulaire et avons constaté que les processus de plasticité normalement altérés dans le cadre d’un TIMP2 réduit étaient désormais restaurés », note le Dr Castellano. « Cette découverte a des implications importantes pour comprendre fondamentalement comment la plasticité est régulée au niveau structurel dans les régions du cerveau impliquées dans la mémoire. »
Dans l’ensemble, les résultats suggèrent que le ciblage des processus qui régulent la matrice extracellulaire pourrait constituer une direction importante pour concevoir des approches améliorant la plasticité du cerveau. Le Dr Castellano, dont le laboratoire se concentre sur la caractérisation des facteurs susceptibles d’inverser les caractéristiques du vieillissement cérébral, prévoit d’explorer des molécules au-delà de TIMP2 qui régulent la matrice extracellulaire, et est optimiste quant aux perspectives que cette recherche pourrait mener dans le contexte de l’atténuation d’un divers troubles liés au vieillissement.
L’étude a été financée par le Instituts nationaux de la santéInstitut National du Vieillissement (R01AG061382, RF1AG072300, T32AG049688).




