Des chercheurs du MIT ont découvert qu’une mutation des microglies, les cellules immunitaires du cerveau, triple le risque de maladie d’Alzheimer. Cette mutation altère la capacité de la microglie à éliminer les débris et à réagir aux lésions neuronales, entraînant une inflammation accrue et un déclin des fonctions cérébrales. Crédit : Issues.fr.com
Une nouvelle étude révèle que les microglies contenant la protéine TREM2 mutante réduisent les connexions des circuits cérébraux, favorisent l’inflammation et contribuent à Alzheimer pathologie par d’autres moyens.
Une mutation génétique rare mais puissante qui altère une protéine des cellules immunitaires du cerveau, connue sous le nom de microglie, peut multiplier par trois le risque de développer la maladie d’Alzheimer. Une nouvelle étude réalisée par des chercheurs du Picower Institute for Learning and Memory à MIT détaille comment la mutation mine la fonction des microglies, expliquant comment elle semble générer ce risque plus élevé.
Aperçus de l’étude sur le dysfonctionnement des microglies
« Cette mutation TREM2 R47H/+ est un facteur de risque assez important pour la maladie d’Alzheimer », explique l’auteur principal de l’étude, Jay Penney, ancien postdoctorant au laboratoire du MIT du professeur Li-Huei Tsai de Picower. Penney est maintenant professeur adjoint à l’Université de l’Île-du-Prince-Édouard. « Cette étude ajoute des preuves claires que le dysfonctionnement des microglies contribue au risque de maladie d’Alzheimer. »
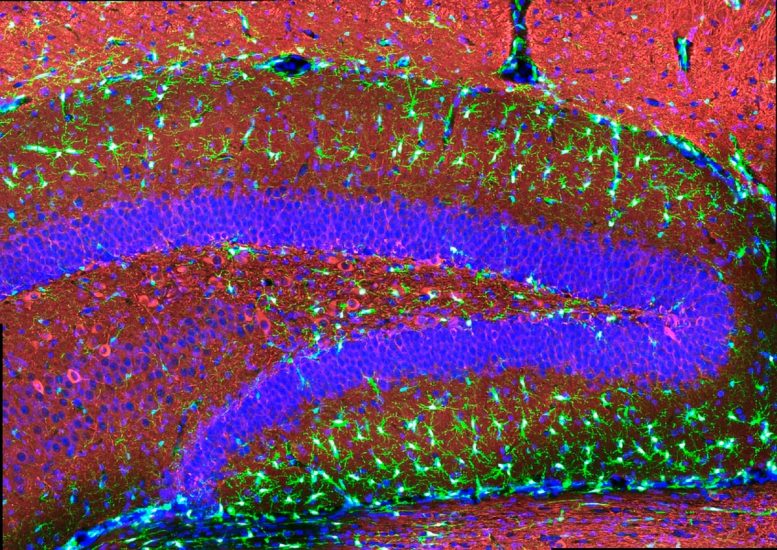
La coloration vert vif met en évidence la microglie humaine implantée dans le tissu de l’hippocampe de souris. Crédit : Jay Penney/Tsai Lab
Dans l’étude publiée dans la revue GLIA, l’équipe de Tsai et Penney montre que les microglies humaines porteuses de la mutation R47H/+ de la protéine TREM2 présentent plusieurs déficits liés à la pathologie d’Alzheimer. Les microglies mutantes sont sujettes à l’inflammation, mais réagissent moins bien aux lésions neuronales et sont moins capables d’éliminer les débris nocifs, y compris la protéine bêta-amyloïde caractéristique de la maladie d’Alzheimer. Et lorsque les scientifiques ont transféré des microglies humaines mutantes TREM2 dans le cerveau de souris, celles-ci ont subi une diminution significative du nombre de synapses, ou de connexions entre leurs neurones, ce qui peut altérer les circuits qui activent les fonctions cérébrales telles que la mémoire.
L’étude n’est pas la première à se demander comment la mutation TREM2 R47H/+ contribue à la maladie d’Alzheimer, mais elle pourrait faire progresser les connaissances émergentes des scientifiques, dit Penney. Les premières études suggéraient que la mutation avait simplement privé la protéine de sa fonction, mais les nouvelles preuves dressent un tableau plus profond et plus nuancé. Bien que les microglies présentent une élimination réduite des débris et une réponse réduite aux blessures, elles deviennent hyperactives d’autres manières, telles que leur inflammation excessive et leur réaction aux blessures. synapse taille.
« Il y a une perte partielle de fonction, mais aussi un gain de fonction pour certaines choses », explique Penney.
Mauvais comportement des microglies
Plutôt que de s’appuyer sur des modèles murins de mutation TREM2 R47H/+, Penney, Tsai et leurs co-auteurs ont concentré leurs travaux sur les cultures de cellules microgliales humaines. Pour ce faire, ils ont utilisé une lignée de cellules souches dérivées de cellules cutanées données par une femme de 75 ans en bonne santé. Dans certaines cellules souches, ils ont ensuite utilisé l’édition génique CRISPR pour insérer la mutation R47H/+, puis ont cultivé des cellules souches modifiées et non modifiées pour devenir des microglies. Cette stratégie leur a fourni un approvisionnement en microglies mutées et en microglies saines, pour servir de contrôles expérimentaux, qui étaient par ailleurs génétiquement identiques.
L’équipe a ensuite examiné comment le fait d’héberger la mutation affectait l’expression de ses gènes dans chaque lignée cellulaire. Les scientifiques ont mesuré plus de 1 000 différences, mais une découverte particulièrement remarquable a été que les microglies porteuses de la mutation augmentaient l’expression de gènes associés à l’inflammation et aux réponses immunitaires. Ensuite, lorsqu’ils ont exposé les microglies en culture à des produits chimiques simulant une infection, la microglie mutante a démontré une réponse significativement plus prononcée que la microglie normale, ce qui suggère que la mutation rend la microglie beaucoup plus sujette à l’inflammation.
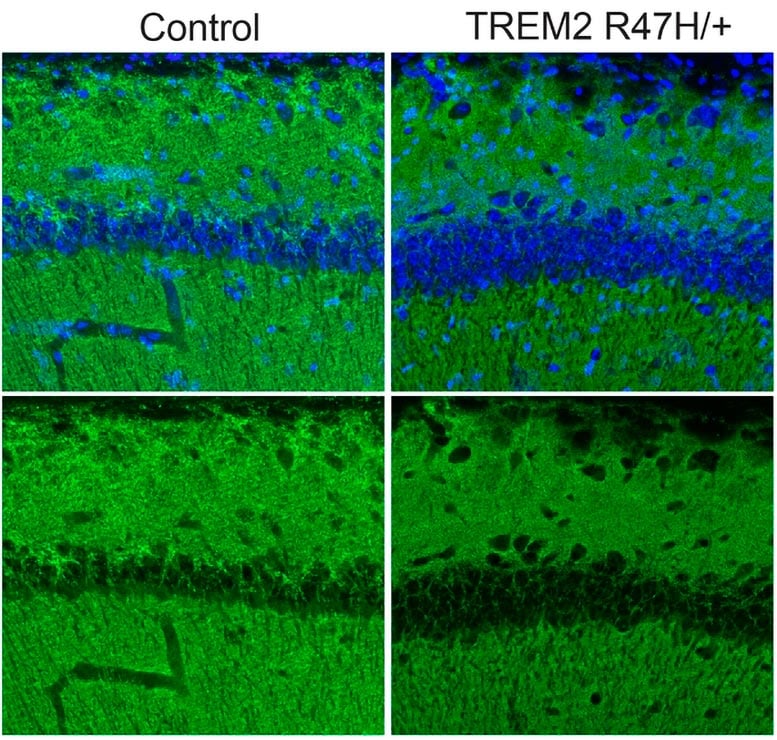
La coloration verte dans le tissu de l’hippocampe de souris indique les niveaux d’une protéine associée aux synapses. La coloration est sensiblement plus brillante chez une souris ayant reçu une microglie humaine saine (témoin) que chez une souris ayant reçu une microglie mutante. Crédit : Jay Penney/Tsai Lab
Dans d’autres expériences avec les cellules, l’équipe les a exposées à trois types de débris microgliaux généralement éliminés dans le cerveau : la myéline, les protéines synaptiques et la bêta-amyloïde. Les microglies mutantes ont moins disparu que les microglies saines.
Une autre tâche de la microglie consiste à réagir lorsque des cellules, telles que les neurones, sont blessées. L’équipe de Penney et Tsai a co-cultivé des microglies et des neurones, puis a détruit les neurones avec un laser. Pendant les 90 minutes qui ont suivi la blessure, l’équipe a suivi le mouvement des microglies environnantes. Par rapport aux microglies normales, les personnes porteuses de la mutation se sont révélées moins susceptibles de se diriger vers la cellule blessée.
Enfin, pour tester comment les microglies mutantes agissent dans un cerveau vivant, les scientifiques ont transplanté des microglies mutantes ou témoins saines chez des souris dans une région du cerveau axée sur la mémoire appelée hippocampe. Les scientifiques ont ensuite coloré cette région pour mettre en évidence diverses protéines d’intérêt. Avoir des microglies humaines mutantes ou normales n’avait pas d’importance pour certaines mesures, mais les protéines associées aux synapses étaient considérablement réduites chez les souris où les microglies mutées étaient implantées.
Qu’est-ce qui fait tiquer la microglie ?
En combinant les preuves des mesures de l’expression génique et celles des expériences sur la fonction microgliale, les chercheurs ont pu formuler de nouvelles idées sur les causes d’au moins une partie du mauvais comportement microglial. Par exemple, l’équipe de Penney et Tsai a remarqué une baisse de l’expression d’une protéine réceptrice « purinergique » impliquant la détection d’une lésion neuronale, expliquant peut-être pourquoi la microglie mutante a eu du mal à accomplir cette tâche. Ils ont également noté que les souris porteuses de la mutation surexprimaient les protéines « complémentaires » utilisées pour marquer les synapses en vue de leur élimination. Cela pourrait expliquer pourquoi les microglies mutantes étaient trop zélées pour éliminer les synapses chez les souris, dit Penney, bien qu’une inflammation accrue puisse également en être la cause en nuisant aux neurones en général.
À mesure que les mécanismes moléculaires sous-jacents au dysfonctionnement microglial deviennent plus clairs, dit Penney, les développeurs de médicaments obtiendront des informations essentielles sur les moyens de cibler le risque de maladie plus élevé associé à la mutation TREM2 R47H/+.
« Nos résultats mettent en évidence les multiples effets de la mutation TREM2 R47H/+ susceptibles d’être à l’origine de son association avec le risque de maladie d’Alzheimer et suggèrent de nouveaux ganglions qui pourraient être exploités pour une intervention thérapeutique », concluent les auteurs.
Outre Penney et Tsai, les autres auteurs de l’article sont William Ralvenius, Anjanet Loon, Oyku Cerit, Vishnu Dileep, Blerta Milo, Ping-Chieh Pao et Hannah Woolf.
La Fondation de la famille Robert A. et Renee Belfer, le Fonds Cure Alzheimer, le Instituts nationaux de la santéLa Fondation JPB, le Picower Institute for Learning and Memory et le Human Frontier Science Program ont financé l’étude.