La gluténine, une protéine de blé, s’avère prometteuse pour la production de viande cultivée en laboratoire en favorisant la culture de couches musculaires et graisseuses qui imitent la texture et la composition de la vraie viande, offrant ainsi une alternative durable à la viande traditionnelle à mesure que la population mondiale augmente.
À mesure que la population mondiale augmente, la viande cultivée en laboratoire, composée de cellules musculaires et adipeuses animales cultivées en laboratoire, présente une solution prometteuse pour répondre à la demande croissante de protéines. De plus, des protéines végétales abordables pourraient servir de base à ces cultures cellulaires. Des découvertes récentes publiées dans ACS Science et ingénierie des biomatériaux démontrent que la gluténine, une protéine de blé non allergène, a réussi à développer des couches musculaires striées et des couches de graisse plates, qui pourraient être combinées pour produire des textures semblables à celles de la viande.
Développement d’échafaudages à base de plantes pour la viande cultivée
Les cellules cultivées ont besoin d’une base ou d’un échafaudage pour adhérer afin de produire de la viande cultivée en laboratoire. Les protéines végétales sont des candidats attrayants pour les échafaudages car elles sont comestibles, abondantes et peu coûteuses. Des chercheurs précédents ont montré qu’un film végétal à base de gluténine constituait une base efficace pour cultiver des cellules musculaires squelettiques de vache.
Mais pour que cette technique produise une alternative prometteuse semblable à la viande, les cellules musculaires doivent former des fibres alignées, similaires à la texture des vrais tissus. De plus, la graisse doit être incluse dans la structure 3D pour reproduire la composition des produits carnés traditionnels. Pour tirer parti de l’utilisation de la gluténine, une protéine du gluten à laquelle les personnes atteintes de la maladie cœliaque ou sensibles au gluten ne réagissent généralement pas, Ya Yao, John Yuen, Jr., Chunmei Li, David Kaplan et leurs collègues ont voulu développer des protéines à base de plantes. des films avec pour développer des cellules musculaires texturées et des couches graisseuses.
Résultats expérimentaux et orientations futures
Les chercheurs ont isolé la gluténine du gluten de blé et formé des films plats et à motifs de crêtes. Ensuite, ils ont déposé des cellules de souris qui se transforment en muscle squelettique sur les bases protéiques et ont incubé les films recouverts de cellules pendant deux semaines. Les cellules se sont développées et ont proliféré sur les films plats et striés. Comme prévu, par rapport aux cellules cultivées sur des films témoins en gélatine, les performances des films à base de gluténine étaient inférieures mais suffisantes. Les chercheurs affirment que des travaux supplémentaires doivent être effectués pour améliorer la manière dont les cellules s’attachent au film végétal afin de se rapprocher de la croissance sur le biomatériau d’origine animale. Au cours de la deuxième semaine de culture, les cellules du film à motifs ont formé de longs faisceaux parallèles, recréant la structure fibreuse des muscles animaux.
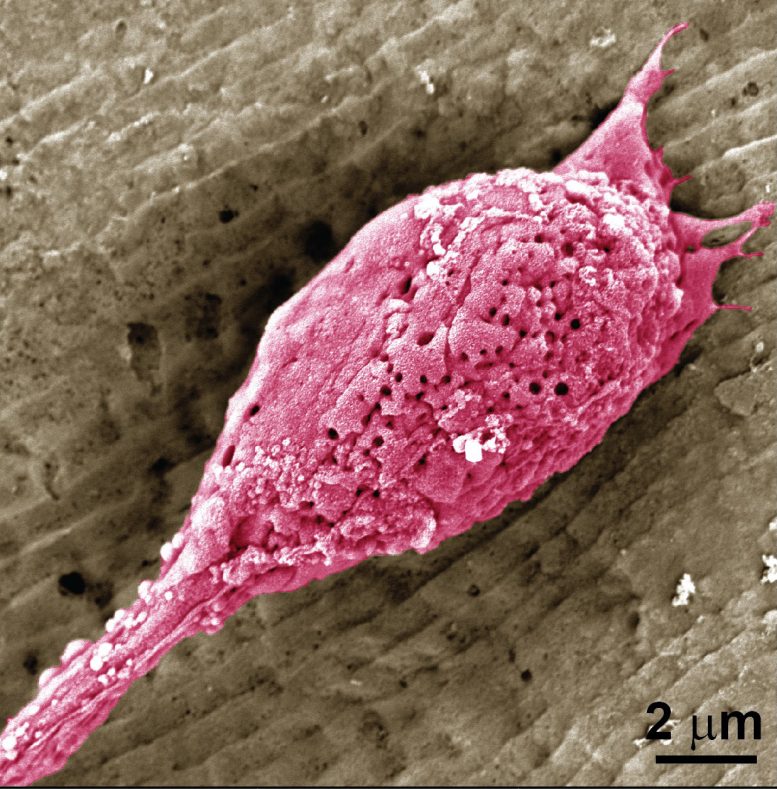
Dans un autre test, des cellules de souris produisant des tissus adipeux ont été déposées sur des films plats de gluténine. Pendant la période d’incubation, à mesure que les cellules proliféraient et se différenciaient, elles produisaient des dépôts visibles de lipides et de collagène.
Les couches de viande et de graisse cultivées attachées aux films de gluténine comestibles pourraient être empilées pour former une protéine alternative 3D semblable à de la viande. Parce que la base matérielle de gluténine a soutenu la croissance à la fois des muscles texturés des animaux et des couches de graisse, les chercheurs affirment qu’elle pourrait être utilisée dans une approche pour des produits carnés cultivés plus réalistes.
Les auteurs reconnaissent le financement de MilliporeSigma et du ministère américain de l’Agriculture. Certains auteurs sont des employés de MilliporeSigma, Inc.




